题目内容
氯、溴、碘、钠、镁、锰、锂、铀等元素在海洋中被富集。海洋开发利用和维权是国家战略。
(1)以上元素在海水中的存在形态是___________(选填①游离态②化合态③不确定)
(2)以下变化属于化学变化的是__________________________:
①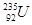 发生核裂变,②重氢(2H)发生核聚变,③LiH做野外生氢剂,④海水晒盐
发生核裂变,②重氢(2H)发生核聚变,③LiH做野外生氢剂,④海水晒盐
(3)由氯气和晒盐后的卤水制取液溴的离子方程式______________________________;由石灰乳和卤水沉淀出镁元素的离子方程式_____________________________________;由海带灰可浸出KI,由某种矿盐可浸出KIO3,二者在盐酸中反应可生成碘单质,反应的离子方程式__________________________________。
(4)工业由氯化钠制取金属钠的化学方程式为____________________________;工业制镁采用电解熔融氯化镁,不采用电解熔融氧化镁的原因是_______________________
(5)海底富集多种矿物结核,锰结核是其中的一种。锰结核中主要含有MnO2和Fe2O3。一种质量比约为m(Mn):m(Fe)=55:448的合金钢(其它元素略),具有抗御激烈冲击和磨损的能力,可做航母甲板等。欲通过铝热反应炼得这样的合金,MnO2、Fe2O3、Al的投料比(按物质的量之比)约为_______________。
(1)以上元素在海水中的存在形态是___________(选填①游离态②化合态③不确定)
(2)以下变化属于化学变化的是__________________________:
①
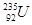 发生核裂变,②重氢(2H)发生核聚变,③LiH做野外生氢剂,④海水晒盐
发生核裂变,②重氢(2H)发生核聚变,③LiH做野外生氢剂,④海水晒盐(3)由氯气和晒盐后的卤水制取液溴的离子方程式______________________________;由石灰乳和卤水沉淀出镁元素的离子方程式_____________________________________;由海带灰可浸出KI,由某种矿盐可浸出KIO3,二者在盐酸中反应可生成碘单质,反应的离子方程式__________________________________。
(4)工业由氯化钠制取金属钠的化学方程式为____________________________;工业制镁采用电解熔融氯化镁,不采用电解熔融氧化镁的原因是_______________________
(5)海底富集多种矿物结核,锰结核是其中的一种。锰结核中主要含有MnO2和Fe2O3。一种质量比约为m(Mn):m(Fe)=55:448的合金钢(其它元素略),具有抗御激烈冲击和磨损的能力,可做航母甲板等。欲通过铝热反应炼得这样的合金,MnO2、Fe2O3、Al的投料比(按物质的量之比)约为_______________。
(1)②
(2)③;
(3)Cl2+2Br-=2Cl-+Br2;Ca(OH)2+Mg2+=Mg(OH)2↓+Ca2+;5I-+IO3-+6H+=3I2+3H2O熔点高,能耗高。
(4)2NaCl 2Na+Cl2↑;MgO熔点高,能耗高。(5)3:12:28 .
2Na+Cl2↑;MgO熔点高,能耗高。(5)3:12:28 .
(2)③;
(3)Cl2+2Br-=2Cl-+Br2;Ca(OH)2+Mg2+=Mg(OH)2↓+Ca2+;5I-+IO3-+6H+=3I2+3H2O熔点高,能耗高。
(4)2NaCl
 2Na+Cl2↑;MgO熔点高,能耗高。(5)3:12:28 .
2Na+Cl2↑;MgO熔点高,能耗高。(5)3:12:28 .试题分析:在海水中各种元素都是以盐即化合物的形式存在。(1)故选②。化学变化的过程是个原子重新的过程。在这个过程中原子的种类、个数不变。不论是核裂变还是核聚变都是核反应,能产生新的元素,海水晒盐是物理变化。(2)选③(3)氧化性Cl2〉Br2,所以会发生反应:Cl2+ 2Br-=2Cl-+Br2石灰乳和卤水中的镁离子发生复分解反应,氢氧化钙是以石灰乳形式存在,书写离子方程式时要写化学式,若以水溶液的形式存在就拆成离子形式。KI和KIO3在酸性条件下会发生氧化还原反应生成碘单质,离子方程式5I-+IO3-+6H+=3I2+3H2O. (4)钠的还原性很强,它的单质只能用电解熔融的氯化钠法制取。MgO、MgCl2虽都是离子化合物,但由于氧化镁的离子键强,熔点高断裂离子键需消耗大量的能量,一般也就用电解熔融氯化镁的方法制取金属镁。(5)n(Mn):n(Fe)=1:8,用铝作还原剂,假设锰物质的量为1mol,根据电子守恒,可得n(Al)=(1×4∕3)mol+8×1mol="(28∕3" )mol。故n(MnO2):n(Fe2O3):n(Al)=1:4:(28∕3)=3:12:28.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目