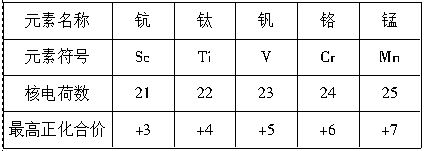
题目内容
下表是元素周期表的一部分,回答下列有关问题:
(1)写出⑦单质分子的化学式 ;画出负2价的 ⑨离子结构示意图 ;
写出⑩单质与水反应的离子方程式: 。
(2) ①~⑩元素中最高价氧化物的水化物碱性最强的是________(填化学式)。
①、③、④简单阳离子按离子半径由大到小的顺序排列为_________(用离子符号表示)。
(3)写出①、⑧元素按1:1的原子比例组成的化合物与⑤的最高价氧化物反应的化学方程式: 。
(4) X元素①~⑩元素中的其一种,其氢氧化物既能溶于氢氧化钠溶液中反应,也能与盐酸反应。
则 :X的元素符号是 ,它位于元素周期表的位置 。
X的氢氧化物与盐酸反应的离子方程式 。
(5)①与③化学性质较活泼的是_____,(元素符号)设计实验证明:________________________________________________________________________________________________________(简述实验操作步骤及现象)
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | ⑤ | ⑦ | ⑧ | | |
| 3 | ① | ③ | ④ | ⑥ | | ⑨ | ⑩ | |
| 4 | ② | | | | | | | |
写出⑩单质与水反应的离子方程式: 。
(2) ①~⑩元素中最高价氧化物的水化物碱性最强的是________(填化学式)。
①、③、④简单阳离子按离子半径由大到小的顺序排列为_________(用离子符号表示)。
(3)写出①、⑧元素按1:1的原子比例组成的化合物与⑤的最高价氧化物反应的化学方程式: 。
(4) X元素①~⑩元素中的其一种,其氢氧化物既能溶于氢氧化钠溶液中反应,也能与盐酸反应。
则 :X的元素符号是 ,它位于元素周期表的位置 。
X的氢氧化物与盐酸反应的离子方程式 。
(5)①与③化学性质较活泼的是_____,(元素符号)设计实验证明:________________________________________________________________________________________________________(简述实验操作步骤及现象)
(15分,方程式及实验描述各2分,其余每空一分每空1分)
(1) N2;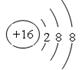 ;Cl2 + H2O = H+ + Cl- + HClO (2)KOH;Na+ >Mg2+>Al3+
;Cl2 + H2O = H+ + Cl- + HClO (2)KOH;Na+ >Mg2+>Al3+
(3)2Na2O2+2CO2==2Na2CO3+O2 (4)Al;第三周期、第IIIA族;Al(OH)3+ 3H+=Al3+ +3H2O
(5) Na 取相同大小的Na和Mg单质,分别投入两支含有等量蒸馏水的试管中,观察到Na反应更加剧烈。
(1) N2;
 ;Cl2 + H2O = H+ + Cl- + HClO (2)KOH;Na+ >Mg2+>Al3+
;Cl2 + H2O = H+ + Cl- + HClO (2)KOH;Na+ >Mg2+>Al3+(3)2Na2O2+2CO2==2Na2CO3+O2 (4)Al;第三周期、第IIIA族;Al(OH)3+ 3H+=Al3+ +3H2O
(5) Na 取相同大小的Na和Mg单质,分别投入两支含有等量蒸馏水的试管中,观察到Na反应更加剧烈。
试题分析:根据元素在周期表中的相对位置可知,①~⑩分别是Na、K、Mg、Al、C、Si、N、O、S、Cl。
(1)⑦单质分子是氮气,其化学式为N2;负2价的 ⑨离子结构示意图是
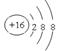 ;氯气与水反应的离子方程式是Cl2 + H2O = H+ + Cl- + HClO。
;氯气与水反应的离子方程式是Cl2 + H2O = H+ + Cl- + HClO。(2)金属性越强,最高价氧化物的水化物的碱性越强,则①~⑩元素中最高价氧化物的水化物碱性最强的是KOH。核外电子排布相同的微粒,其微粒半径随原子序数的增大而减小,则①、③、④简单阳离子按离子半径由大到小的顺序排列为Na+ >Mg2+>Al3+。
(3)①、⑧元素按1:1的原子比例组成的化合物是过氧化钠,⑤的最高价氧化物是CO2,则二者反应的化学方程式是2Na2O2+2CO2==2Na2CO3+O2。
(4)氢氧化铝是两性氢氧化物,既能溶于氢氧化钠溶液中反应,也能与盐酸反应,所以X是Al。位于第三周期第IIIA族;氢氧化铝和盐酸反应的离子方程式是Al(OH)3+ 3H+=Al3+ +3H2O。
(5)同周期自左向右金属性逐渐减弱,则①与③化学性质较活泼的Na。比较金属性强弱,可以依据金属单质与水反应的难易程度很累验证,则正确的操作是取相同大小的Na和Mg单质,分别投入两支含有等量蒸馏水的试管中,观察到Na反应更加剧烈。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和应试能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力,考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。有利于培养学生的逻辑推理能力和发散思维能力以及规范严谨的答题能力。

练习册系列答案
相关题目