题目内容
下列实验现象所对应的离子方程式不正确的是
| | 实 验 | 现 象 | 离子方程式 |
| A |  | 在空气中放置一段时间后溶液呈蓝色 | 4H+ + 4I- + O2 ="=" 2I2 + 2H2O |
| B |  | 开始时无气泡,后来有气泡 | CO32-+H+=HCO3- HCO3-+H+ ="=" H2O+CO2↑ |
| C |  | 溶液由黄绿色变为无色 | Cl2 + 2OH- ="=" Cl- + ClO- + H2O |
| D |  | 有白色沉淀生成,溶液由红色变为无色 | Ba2++OH-+H++SO42-="=" BaSO4↓+H2O |
D
试题分析:A、I-在酸性条件下与空气中的氧气发生氧化还原反应生成碘,溶液变蓝,正确;B、稀盐酸滴入碳酸钠溶液中,盐酸少量,开始生成碳酸氢钠,无气泡产生,继续滴加,盐酸与碳酸氢钠反应产生二氧化碳气体,正确;C、氯水呈黄绿色,加入氢氧化钠溶液后溶液为无色,是因为氯水中的氯气与氢氧化钠反应,氯气消失,溶液黄绿色消失,正确;D、离子方程式中的阴阳离子之比不符合氢氧化钡与硫酸的化学式中的阴阳离子之比,错误,答案选D。

练习册系列答案
相关题目
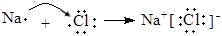
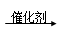 2CO2 +N2
2CO2 +N2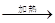 CH3COO-+NH4++2Ag↓+3NH3+H2O
CH3COO-+NH4++2Ag↓+3NH3+H2O


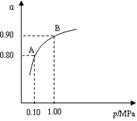
 2SO3(g);△H<0,550 ℃时,SO2转化为SO3的平衡转化率(α)与体系总压强(p)的关系如图所示。
2SO3(g);△H<0,550 ℃时,SO2转化为SO3的平衡转化率(α)与体系总压强(p)的关系如图所示。