题目内容
下列电子式中正确的是
A. | B. | C. | D. |
B
CO2中碳和氧形成的是双键,电子式为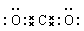 。氨气中氮原子还有1对电子没有参与成键,电子式为
。氨气中氮原子还有1对电子没有参与成键,电子式为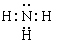 。四氯化碳中每个氯原子还有3对电子没有参与成键,电子式为
。四氯化碳中每个氯原子还有3对电子没有参与成键,电子式为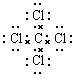 。所以正确的答案是B。
。所以正确的答案是B。
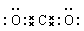 。氨气中氮原子还有1对电子没有参与成键,电子式为
。氨气中氮原子还有1对电子没有参与成键,电子式为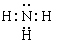 。四氯化碳中每个氯原子还有3对电子没有参与成键,电子式为
。四氯化碳中每个氯原子还有3对电子没有参与成键,电子式为 。所以正确的答案是B。
。所以正确的答案是B。
练习册系列答案
相关题目
题目内容
A. | B. | C. | D. |
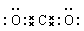 。氨气中氮原子还有1对电子没有参与成键,电子式为
。氨气中氮原子还有1对电子没有参与成键,电子式为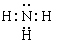 。四氯化碳中每个氯原子还有3对电子没有参与成键,电子式为
。四氯化碳中每个氯原子还有3对电子没有参与成键,电子式为 。所以正确的答案是B。
。所以正确的答案是B。