题目内容
12.下列事实与氢键有关的是( )| A. | HF、HCl、HBr、HI的热稳定性依次减弱 | |
| B. | 水加热到很高的温度都难以分解 | |
| C. | CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高 | |
| D. | 水结成冰体积膨胀 |
分析 A.非金属性越强,对应氢化物越稳定;
B.水加热到很高的温度都难以分解,可知水很稳定;
C.由分子构成的物质中,相对分子质量越大,沸点越大;
D.水结成冰,冰晶体中的水分子的空间利用率不高,留有相当大的空隙.
解答 解:A.HF、HCl、HBr、HI的热稳定性与F、Cl、Br、I的非金属性有关,非金属性越强,其氢化物越稳定,同一主族的元素,非金属性随着原子序数的增加而减小,所以其氢化物的热稳定性逐渐减弱,与氢键无关,故A不选;
B.水的分解需要破坏的是化学键,与化学键有关,与氢键无关,故B不选;
C.CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高,与分子间作用力有关,与氢键无关,故C不选;
D.氢键具有方向性,氢键的存在迫使四面体中心的每个水分子与四面体顶角方向的4个相邻水分子相互吸引,这一排列使冰晶体中的水分子的空间利用率不高,留有相当大的空隙,所以水结成冰时,体积增大,与氢键有关,故D选;
故选D.
点评 本题考查氢键及物质的性质,为高频考点,把握稳定性与化学键有关、氢键影响物理性质为解答的关键,侧重分析与应用能力的考查,注意选项B为易错点,题目难度不大.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
3. 如图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
如图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
 如图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
如图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )| A. | 原子半径:W>Z>Y>X | |
| B. | 气态氢化物的稳定性:Z>W>X>Y | |
| C. | W的最高正化合价与负化合价的绝对值可能相等 | |
| D. | 若X位于第VA族,则沸点:XH3<WH3 |
20.下列物质在变化过程中,化学键没有被破坏的是( )
| A. | 干冰升华 | B. | 食盐溶解 | ||
| C. | 氯化铵受热,固体消失 | D. | 电解水 |
7.下列说法正确的是( )
| A. | 淀粉、油脂及其水解产物均不属于电解质 | |
| B. | 葡萄糖可用于补钙药物制剂的合成 | |
| C. | 石油是复杂的混合物,其分馏产物为纯净物 | |
| D. | 天然气的产量用来衡量一个国家石油化工的发展水平 |
17.有机物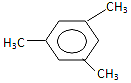 用系统命名法命名的名称为( )
用系统命名法命名的名称为( )
 用系统命名法命名的名称为( )
用系统命名法命名的名称为( )| A. | 间三甲苯 | B. | 1,3,5-三甲苯 | C. | 三甲苯 | D. | 1-3-5,三甲苯 |
7.已知: ,且烷烃满足下列条件:
,且烷烃满足下列条件:
①主链含5个碳原子 ②两个支链:一个甲基、一个乙基,n、m的最大值分别为( )
 ,且烷烃满足下列条件:
,且烷烃满足下列条件:①主链含5个碳原子 ②两个支链:一个甲基、一个乙基,n、m的最大值分别为( )
| A. | 2、2 | B. | 2、4 | C. | 4、2 | D. | 4、5 |
8.今有两种正盐的稀溶液,分别是a mol/LNaX溶液和b mol/LNaY溶液,下列说法不正确的是( )
| A. | 若a>b,且c(X-)=c(Y-),则相同浓度时,酸性HX<HY | |
| B. | 若a=b,pH(NaX)>pH(NaY),则相同条件时,酸性HX<HY | |
| C. | 若a=b,且c(X-)=c(Y-)+c(HY),则相同条件时,酸性HX<HY | |
| D. | 若等体积混合,且c(X-)+c(Y-)+c(HX)+c(HY)=0.1mol/L,则一定有a+b=0.2mol/L |
