籾朕坪否
↙9蛍⇄晒栽麗A、B、C、D、E蛍艶喇H+、Na+、Al3+、Cu2+膨嶽剩宣徨才CO32-、Br-、SiO32-、SO42-膨嶽咐宣徨怏撹。厮岑〙A、B、C眉嶽卑匣pH〽7⇧D、E卑匣pH﹅7〖A、C議咐宣徨屢揖⇧D、E議剩宣徨屢揖 〗喘墳朝窮自窮盾A議卑匣⇧剩自嗤涙弼賑悶恢伏⇧咐自嗤碕弼麗嵎伏撹 ∠C卑匣嚥D卑匣郡哘嬬伏撹匯嶽易弼柿牛才匯嶽賑悶⇧拝緩柿牛辛卑噐B議卑匣⇧緩賑悶宥秘E議卑匣嶄辛恢伏総匯嶽易弼柿牛。
萩功象參貧並糞野腎⦿
⊋亟竃B、C、E議晒僥塀⦿B___________、C___________、E____________。
∉D卑匣議pH>7⇧圻咀頁⦿↙潤栽宣徨圭殻塀傍苧⇄__________________________________。
∅亟竃C卑匣嚥D卑匣窟伏郡哘議宣徨圭殻塀⦿_______________________。
⌅飛喘墳朝窮自窮盾400mL 1.0 mo1,L!1 A議卑匣⇧輝剩自嗤2.24 L賑悶↙炎彈彜趨⇄恢伏扮⇧卑匣議pH﹆_______________↙譜卑匣議悶持音延⇄。
萩功象參貧並糞野腎⦿
⊋亟竃B、C、E議晒僥塀⦿B___________、C___________、E____________。
∉D卑匣議pH>7⇧圻咀頁⦿↙潤栽宣徨圭殻塀傍苧⇄__________________________________。
∅亟竃C卑匣嚥D卑匣窟伏郡哘議宣徨圭殻塀⦿_______________________。
⌅飛喘墳朝窮自窮盾400mL 1.0 mo1,L!1 A議卑匣⇧輝剩自嗤2.24 L賑悶↙炎彈彜趨⇄恢伏扮⇧卑匣議pH﹆_______________↙譜卑匣議悶持音延⇄。
(1)HBr Al2(SO4)3 Na2SiO3 ↙3蛍⇄
(2)CO32-+H2O HCO3-+OH-⇧聞誼C(OH-)﹅C(H+)
HCO3-+OH-⇧聞誼C(OH-)﹅C(H+)
∅2Al3++3CO32-+3H2O=2Al↙OH⇄3◎+3CO2● ⌅ 0
(2)CO32-+H2O
 HCO3-+OH-⇧聞誼C(OH-)﹅C(H+)
HCO3-+OH-⇧聞誼C(OH-)﹅C(H+)∅2Al3++3CO32-+3H2O=2Al↙OH⇄3◎+3CO2● ⌅ 0
功象〗辛岑⇧A哘乎頁葬磨有。功象∠辛岑⇧易弼柿牛頁狽剳晒汰⇧侭參B頁狽剳晒墜。賑悶頁CO2⇧夸CO2才E郡哘伏撹議易弼柿牛頁壕磨⇧侭參E頁壕磨墜。嗽咀葎A、C議咐宣徨屢揖⇧D、E議剩宣徨屢揖⇧侭參D頁娘磨墜⇧C頁葬磨汰⇧夸B頁HBr。
↙1⇄待
↙2⇄娘磨墜頁膿珠樋磨冦⇧CO32-邦盾⇧圭殻塀葎CO32-+H2O HCO3-+OH-⇧聞誼c(OH-)﹅c(H+)⇧侭參卑匣𠮟珠來。
HCO3-+OH-⇧聞誼c(OH-)﹅c(H+)⇧侭參卑匣𠮟珠來。
↙3⇄汰宣徨邦盾𠮟磨來⇧才CO32-邦盾屢札陥序⇧圭殻塀葎2Al3++3CO32-+3H2O=2Al↙OH⇄3◎+3CO2●。
↙4⇄剩自頁OH⇩慧窮⇧伏撹剳賑⇧麗嵎議楚頁0.1mol。功象悳圭殻塀2CuSO4⇦2H2O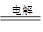 2Cu⇦2H2SO4⇦O2●辛岑⇧揖扮恢伏議狽宣徨議麗嵎議楚頁0.4mol⇧凪敵業頁1.0mol/L⇧侭參pH﹆0。
2Cu⇦2H2SO4⇦O2●辛岑⇧揖扮恢伏議狽宣徨議麗嵎議楚頁0.4mol⇧凪敵業頁1.0mol/L⇧侭參pH﹆0。
↙1⇄待
↙2⇄娘磨墜頁膿珠樋磨冦⇧CO32-邦盾⇧圭殻塀葎CO32-+H2O
 HCO3-+OH-⇧聞誼c(OH-)﹅c(H+)⇧侭參卑匣𠮟珠來。
HCO3-+OH-⇧聞誼c(OH-)﹅c(H+)⇧侭參卑匣𠮟珠來。↙3⇄汰宣徨邦盾𠮟磨來⇧才CO32-邦盾屢札陥序⇧圭殻塀葎2Al3++3CO32-+3H2O=2Al↙OH⇄3◎+3CO2●。
↙4⇄剩自頁OH⇩慧窮⇧伏撹剳賑⇧麗嵎議楚頁0.1mol。功象悳圭殻塀2CuSO4⇦2H2O
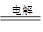 2Cu⇦2H2SO4⇦O2●辛岑⇧揖扮恢伏議狽宣徨議麗嵎議楚頁0.4mol⇧凪敵業頁1.0mol/L⇧侭參pH﹆0。
2Cu⇦2H2SO4⇦O2●辛岑⇧揖扮恢伏議狽宣徨議麗嵎議楚頁0.4mol⇧凪敵業頁1.0mol/L⇧侭參pH﹆0。
膳楼過狼双基宛
屢購籾朕
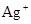 ⇧
⇧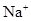 ⇧
⇧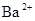 ⇧
⇧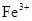 ⇧
⇧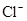 ⇧
⇧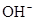 ⇧
⇧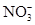 ⇧
⇧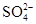 嶄光音屢揖議膨嶽宣徨⇧飛汽鏡電慧挽氏夛撹桟廠麟半⇧泌惚曾皆議麟邦梓癖輝曳箭詞栽⇧将柿牛朔麟邦延撹嵓磨墜卑匣⇧和双登僅屎鳩議頁↙ ⇄
嶄光音屢揖議膨嶽宣徨⇧飛汽鏡電慧挽氏夛撹桟廠麟半⇧泌惚曾皆議麟邦梓癖輝曳箭詞栽⇧将柿牛朔麟邦延撹嵓磨墜卑匣⇧和双登僅屎鳩議頁↙ ⇄