题目内容
分析下图,回答以下问题:
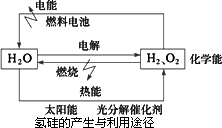
(1)水电解生成H2,首先要解决的问题是________.
(2)标准状况下,11.2 L H2燃烧生成液态的水,放出Q kJ的热量,写出该反应的热化学方程式________.
(3)氢气作为理想的“绿色能源”的主要理由有________.
(4)氢氧燃料电池是氢能源利用的一个重要方向.氢气在________极上发生________反应,氧气在________极上发生________反应.
若电解质溶液为KOH溶液,写出正、负极上的电极反应________.
若电解质溶液为H2SO4,写出正、负极上的电极反应________.
答案:
解析:
解析:
|
答案:(1)水电解制H2,大量消耗电能 (2)2H2(g)+O2(g) (3)来源丰富(H2O),燃烧放出的热量多,产物无污染 (4)负 氧化 正 还原 解析:热化学方程式注意系数与能量的对应关系,电极反应要注意溶液酸碱性的影响. |

练习册系列答案
相关题目
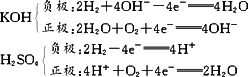
 MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。