题目内容
【题目】镁粉和铝粉分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图,下列说法正确的是( ) 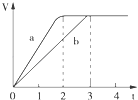
A.镁粉和铝粉的物质的量之比为3:2
B.镁粉和铝粉质量之比为3:2
C.镁粉和铝粉的摩尔质量之比为2:3
D.镁粉和铝粉反应完所需时间之比为3:2
【答案】A
【解析】解:硫酸过量,Mg、Al完全反应,由图可知生成氢气体积相同,则氢气物质的量相等,假设氢气为1mol,根据电子转移守恒,Mg的物质的量为 ![]() =1mol、Al物质的量为
=1mol、Al物质的量为 ![]() =
= ![]() mol. A.Mg、Al的物质的量之比为1mol:
mol. A.Mg、Al的物质的量之比为1mol: ![]() mol=3:2,故A正确;
mol=3:2,故A正确;
B.Mg、Al的质量之比为1mol×24g/mol: ![]() mol×27g/mol=4:3,故B错误;
mol×27g/mol=4:3,故B错误;
C.Mg、Al的摩尔质量之比为24g/mol:27g/mol=8:9,故C错误;
D.金属性Mg>Al,故Mg与盐酸反应速率更快,则镁粉和铝粉反应完所需时间之比为2:3,故D错误,
故选:A.

练习册系列答案
相关题目