题目内容
如下图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质缓缓地压到甲针筒内,进行下表所列的不同实验(气体体积在常温常压下测定)。

|
实验序号 |
甲针筒内物质 |
乙针筒内物质 |
甲针筒的现象 |
|
1 |
40 mL HCl |
40 mL NH3 |
产生白烟 |
|
2 |
40 mL Cl2 |
10mL 水 |
剩余气体为20mL |
|
3 |
30 mL NO |
15 mL O2 |
|
|
4 |
20 mL AlCl3溶液 |
10 mL NaOH溶液 |
生成白色沉淀,后消失 |
(1)如果实验1甲针筒内改装30 mL Cl2 ,乙针筒内仍为40 mL NH3,实验时,甲针筒内也有白烟产生。写出有关反应的化学方程式 。
(2)由实验2可知,常温常压下氯气在水中的溶解度为 。
(3)实验3 反应后甲针筒内气体的体积为 。
(4)实验4中,AlCl3溶液浓度为0.1mol/L,如果最后白色沉淀全部消失,则NaOH溶液浓度至少为 mol/L。
(5)将上述装置做以下改进:在甲、乙针筒之间连接一段硬质玻璃管,如下图。在A处装一种浅黄色的粉末,乙针筒内是一种常见的气体,甲针筒无气体。将乙针筒内气体压入甲针筒内,发现气体体积是原来的一半。A处的物质是 ,甲针筒内的气体为 。

(6)有学生用上述改进后的装置测定空气中氧气的体积分数(加热用酒精灯未画出)。乙针筒内装有50 mL空气。实验时,用酒精灯对A处物质进行加热,经反复慢慢推拉两针筒的活塞,反应完毕,恢复至室温,测得剩余气体为40.5mL。
①A处的物质是 (选填编号)。
a.碳粉 b.二氧化锰 c.铜粉 d.氧化铜
②已知空气中氧气的体积分数为0.2,则该实验的相对误差为 。
(1)3Cl2+4NH3¾®N2+2NH4Cl+4HCl (2分) (写成3Cl2+2NH3¾®N2+6HCl; HCl + NH3¾®NH4Cl或3Cl2+8NH3¾®N2+6NH4Cl得1分;只写3Cl2+2NH3¾®N2+6HCl不得分)
(2)2(或1:2或1体积水溶解2体积氯气。合理即可)(1分)
(3)15 mL<V<30 mL (2分)(只写小于30 mL得1分)
(4)0.8 mol/L(2分)
(5)过氧化钠或Na2O2 (1分) 氧气或O2(1分)
(6)① c. (1分) ②-0.05 或-5%(2分)(没有负号不得分)
【解析】
试题分析:(1)氯气和氨气发生氧化还原反应,氯气氧化氨气为氮气,氯气被还原为氯化氢气体,依据定量关系可知氨气过量一部分,氯化氢和氨气反应生成氯化铵是固体颗粒,冒白烟;反应的化学方程式为:3Cl2+4NH3=N2+2NH4Cl+4HCl;
(2)40mL Cl2在10mL水溶解,最后剩余气体为20mL,则依据气体体积比表示的溶解度为1:2;
(3)30mL NO与15mL O2混合发生反应2NO+O2=2NO2,所以前后反应生成二氧化氮气体体积为30ml,又二氧化氮可以聚合为四氧化二氮气体2NO2⇌N2O4,但反应是可逆反应不能全部转化,所以最后容器中的气体体积介于15ml~30ml;
(4)AlCl3溶液浓度为0.1mol/L,如果最后白色沉淀全部消失,氢氧化钠和氯化铝反应生成氢氧化铝沉淀,氢氧化钠过量会溶解氢氧化铝,沉淀恰好溶解反应的离子方程式为:
所以得到
Al3+ + 4OH- =Al(OH)4-
1 4
0.1mol/L×0.02L c(OH-)×0.01L
计算得到c(NaOH)=0.8mol/L;
(5)在甲、乙针筒之间连接一段硬质玻璃管,如下图.在A处装一种浅黄色的粉末,乙针筒内是一种常见的气体,甲针筒无气体.将乙针筒内气体压入甲针筒内,发现气体体积是原来的一半.A处的物质依据颜色和与气体反应的性质可知,为Na2O2;乙中气体为二氧化碳,和过氧化钠反应后生成气体为氧气,2Na2O2+CO2=2Na2CO3+O2
(6)①测定空气中氧气的体积分数是利用空气中氧气反应,其他气体不反应;
a.碳粉和氧气反应生成二氧化碳,不能测定气体体积变化后氧气的体积,故a不符合;
b.二氧化锰不能和空气中 氧气反应,不能测定,故B不符合;
c.铜粉和氧气反应生成氧化铜,可以测定气体减小,计算氧气的条件分数,故C符合;
d.氧化铜不能和空气中氧气反应,不能测定体积分数,故d不符合;故选c.
②乙针筒内装有50mL空气。实验时,用酒精灯对A处物质进行加热,经反复慢慢推拉两针筒的活塞,反应完毕,恢复至室温,测得剩余气体为40.5mL.体积变化为氧气=50ml-40.5ml=9.5ml,氧气体积分数=9.5ml/50ml×100%=0.19,所以相对误差=(0.2-0.19)÷0.2×100%=5%,故答案为:-5%
考点:本题考查的是氨气、氯气、氮的化合物过氧化钠等物质的性质应用,实验现象分析和定量计算是考查重点,掌握基础是解题关键,题目难度中等.

 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案(A)如下图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定)。
![]()
实验序号 | 甲针筒内物质 | 乙针筒内物质 | 甲针筒的现象 |
1 | 10 mL FeSO4溶液 | 10 mL NH3 | 生成白色沉淀,后变色 |
2 | 20 mL H2S | 10 mL SO2 |
|
3 | 30 mL NO2(主要) | 10 mL H2O(l) | 剩有无色气体,活塞自动向内压缩 |
4 | 15 mL Cl2 | 40 mL NH3 |
|
试回答下列问题:
(1)实验1中,沉淀最终变为___________色,写出沉淀变色的化学方程式_______________。
(2)实验2甲针筒内的现象是:有________生成,活塞___________移动(填“向外”“向内”或“不”)。反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入__________溶液中。
(3)实验3中,甲中的30 mL气体是NO2和N2O4的混合气体,那么甲中最后剩余的无色气体是__________,写出NO2与H2O反应的化学方程式_______________________________。
(4)实验4中,已知:3Cl2+2NH3![]() N2+6HCl。甲针筒除活塞有移动、针筒内有白烟产生外,气体的颜色变化为___________,最后针筒内剩余气体的体积约为______________mL。
N2+6HCl。甲针筒除活塞有移动、针筒内有白烟产生外,气体的颜色变化为___________,最后针筒内剩余气体的体积约为______________mL。
(B)某实验小组用下列装置进行乙醇催化氧化的实验。

(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学反应方程式
_____________________________________________________________________
_____________________________________________________________________。
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是________反应。
(2)甲和乙两个水浴作用不相同。
甲的作用是____________________;乙的作用是_____________________。
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是____________________________。集气瓶中收集到的气体的主要成分是______________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有__________。要除去该物质,可先在混合液中加入______________(填写字母)。
a.氯化钠溶液 b.苯
c.碳酸氢钠溶液 d.四氯化碳
然后,再通过_____________(填实验操作名称)即可除去。
如下图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定)。试回答下列问题:
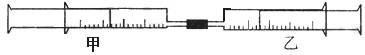
| 实验序号 | 甲针筒内物质 | 乙针筒内物质 | 甲针筒的现象 |
| 1 | 10mLFeSO4溶液 | 10mLNH3 | 生成白色沉淀,后变色 |
| 2 | 20mLH2S | 10mLSO2 | |
| 3 | 30mLNO2(主要) | 10mLH2O(l) | 剩有无色气体,活 塞自动向内压缩 |
| 4 | 15molCl2 | 40mLNH3 |
⑴实验1中,沉淀最终变为 色,写出沉淀变色的化学方程式 。
⑵实验2甲针筒内的现象是:有 生成,活塞 移动(填向外、向内、不)。反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入 溶液中。
⑶实验3中,甲中的30mL气体是NO2和N2O4的混合气体,那么甲中最后剩余的无色气体是 ,写出NO2与H2O反应的化学方程式 。
⑷实验4中,已知:3Cl2+2NH3→N2+6HCl。甲针筒除活塞有移动,针筒内有白烟产生外,气体的颜色变化为 ,最后针筒中剩余气体的体积约为 mL。

