题目内容
(11分)有一包白色固体粉末,其中可能含有KCl、BaCl2、Cu(NO3)2、K2CO3中的一种或几种,现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色:
②向①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液加入足量AgNO3溶液,产生白色沉淀。
试根据上述实验事实,回答下列问题:
(1)写出原白色粉末中一定含有的物质的化学式
(2)写出原白色粉末中一定不含有的物质的电离方程式
(3)写出下列各步变化的离子方程式:
②
④
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色:
②向①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液加入足量AgNO3溶液,产生白色沉淀。
试根据上述实验事实,回答下列问题:
(1)写出原白色粉末中一定含有的物质的化学式
(2)写出原白色粉末中一定不含有的物质的电离方程式
(3)写出下列各步变化的离子方程式:
②
④
(1) BaCl2、K2CO3 (2) Cu(NO3)2=Cu2++2NO3- (3)② BaCO3+2H+=Ba2++CO2↑+H2O ④ Ag++Cl-=AgCl↓
试题分析:将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色,说明固体中没有Cu(NO3)2。向①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生,说明固体中有K2CO3和BaCl2。取少量②的溶液,滴入稀硫酸,有白色沉淀产生,说明固体中有BaCl2,另取①中过滤后的溶液加入足量AgNO3溶液,产生白色沉淀,说明溶液中含有Cl-,KCl、BaCl2至少含有一种。所以固体中一定含有的是K2CO3和BaCl2,一定不含的是Cu(NO3)2,可能含有的是KCl。
点评:本题属于通过离子反应来确定物质的组成,这类习题在08、09年的高考题中都有出现,应该重视。

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
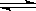 Na++H++SO42一
Na++H++SO42一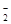 、Na+、Cl-,则Na2O2、HCl和Al2O3的物质的量之可能为( )
、Na+、Cl-,则Na2O2、HCl和Al2O3的物质的量之可能为( )