题目内容
【题目】如图所示,a、b、c均为石墨电极,d为铁电极,通电进行电解。假设在电解过程中产生的气体全部逸出,下列说法正确的是( )
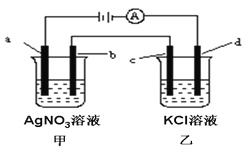
A.乙烧杯中的d电极反应式为Fe-2e-=Fe2+
B.电解一段时间后,将甲、乙两溶液混合,一定会产生沉淀
C.当b极增重5.4g时,d极产生的气体为2.24L(标况)
D.甲烧杯中溶液的pH降低
【答案】D
【解析】
试题分析:A.乙烧杯中的d电极做阴极,电极材料不参加反应。B.电解一段时间,甲可能是硝酸溶液,乙可能是氢氧化钾溶液,混合后无沉淀。 C.当b极增重5.4g时,生成0.05molAg,2molAg——2mole- ---1molH2,d电极可以生成5.6L氢气。D.甲烧杯电解一段时间后生成硝酸,溶液的pH降低。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
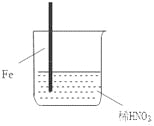
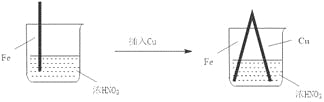
【题目】在通风橱中进行下列实验:
步骤 |
|
| |
现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
下列说法中不正确的是:
A. Ⅰ种气体有无色变红棕色的化学方程式为:2NO+O2=2NO2
B. Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C. 对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D. 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化