题目内容
恒温下,欲使CH3COONa稀溶液中
比值增大,可在溶液中加入少量下列物质中的( )
①NaOH固体
②KOH固体
③KHSO4固体
④CH3COONa固体.
| c(CH3COO-) |
| c(Na+) |
①NaOH固体
②KOH固体
③KHSO4固体
④CH3COONa固体.
| A、②④ | B、③④ | C、①③ | D、①② |
分析:醋酸钠溶液中存在醋酸根离子水解平衡:CH3COO-+H2O?CH3COO-+OH-,影响水解平衡移动的因素来回答判断.
解答:解:①加入NaOH固体,会导致钠离子浓度增大,水解平衡向逆向移动,所以醋酸根离子浓度增大,但是钠离子增加的程度大,即比值会减小,故①错误;
②加入KOH固体,钠离子浓度不变,水解平衡向逆向移动,所以醋酸根离子浓度增大,即比值会增大,故②正确;
③加入KHSO4固体,钠离子浓度不变,水解平衡向正向移动,所以醋酸根离子浓度减小,即比值会减小,故③错误;
④加入CH3COONa固体,醋酸根离子以及钠离子浓度均增大,同时会对水解平衡起到抑制作用,所以醋酸根离子浓度增加的程度大,比值增大,故④正确.
故选:A.
②加入KOH固体,钠离子浓度不变,水解平衡向逆向移动,所以醋酸根离子浓度增大,即比值会增大,故②正确;
③加入KHSO4固体,钠离子浓度不变,水解平衡向正向移动,所以醋酸根离子浓度减小,即比值会减小,故③错误;
④加入CH3COONa固体,醋酸根离子以及钠离子浓度均增大,同时会对水解平衡起到抑制作用,所以醋酸根离子浓度增加的程度大,比值增大,故④正确.
故选:A.
点评:本题考查学生盐的水解原理以及影响盐的水解平衡移动等方面的知识,注意知识的归纳整理是解题关键,难度不大.

练习册系列答案
相关题目

 2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:

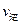 (填“>”、“<”或“=”)
(填“>”、“<”或“=”) )
)