题目内容
25 ℃时,将两个铂电极插入一定量的Na2SO4饱和溶液中进行电解。通电一段时间后,在阴极逸出a mol气体,同时有W g Na2SO4·10H2O晶体析出。若温度保持不变,剩余溶液中溶质的质量分数为( )A.![]() % B.
% B.![]() %
%
C.![]() % D.
% D.![]() %
%
解析:用铂电极电解Na2SO4溶液,两极发生的反应为:
阴极:4H++4e-====2H2↑
阳极:4OH--4e-====2H2O+O2↑
电解的总反应式为:2H2O![]() 2H2↑+O2↑,阴极放出a mol H2,水被电解了a mol,析出的W g Na2SO4·10 H2O中含Na2SO4:W g×
2H2↑+O2↑,阴极放出a mol H2,水被电解了a mol,析出的W g Na2SO4·10 H2O中含Na2SO4:W g×![]() ,析出的Na2SO4·10H2O和被电解了的H2O组合在一起就是饱和Na2SO4溶液,所以:
,析出的Na2SO4·10H2O和被电解了的H2O组合在一起就是饱和Na2SO4溶液,所以:
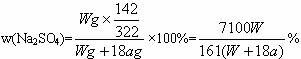
答案:C

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目