题目内容
电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率
变化可以确定滴定反应的终点。右图是KOH溶液分别滴定HCl溶
液和CH3COOH溶液的滴定曲线示意图。下列示意图中,能正确表
示用NH3·H2O溶液滴定HCl和CH3COOH混合溶液的滴定曲线的是( )
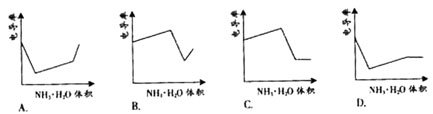
D
解析:
1.HCl为强电解质,HAc为弱电解质,滴加NH3·H2O弱电解质先与HCl反应,生成同样为强电解质的NH4Cl,但溶液体积不断增大,溶液稀释,所以电导率下降。
2.当HCl被中和完后,继续与HAc弱电解质反应,生成NH4Ac的强电解质,所以电导率增大。
3.HCl与HAc均反应完后,继续滴加NH3·H2O弱电解质,电导率变化不大,因为溶液被稀释,有下降趋势。
综上所述:答案选D。

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目