题目内容
近年来全世界经历了多种传染性疾病(如非典、疯牛病、高致病性禽流感等)的袭扰,因此,经常性地对环境进行消毒,是预防各种传染性疾病的有效措施。某研究小组为制备消毒液(主要成分是NaClO),设计了A、B两套装置(B装置中电极材料均为石墨)。并查阅到下列资料:在加热的情况下卤素单质和碱液发生如下反应:3X2+6OH-![]() 5X-+
5X-+![]() +3H2O
+3H2O
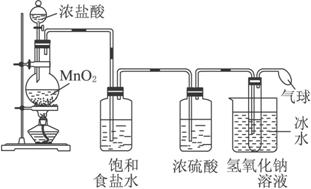
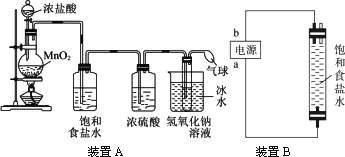
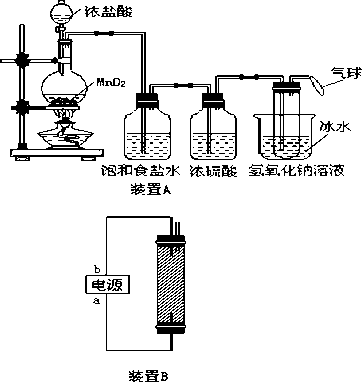
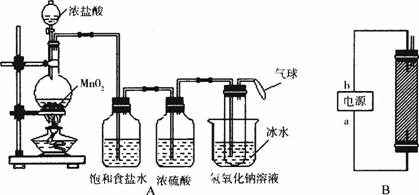
装置A
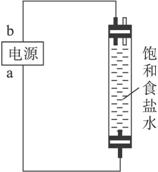
装置B
请完成下列问题:
(1)写出装置A烧瓶中发生反应的化学方程式________________________________ 。
(2)若去掉装置A中盛浓硫酸的洗气瓶,能否达到预期目的_________(填“能”或“不能”)。
(3)装置A中盛冰水的烧杯的作用是_________________________________________。
(4)利用装置B制备消毒液时有关反应的化学方程式为__________________________。
(5)装置B中a端应接电源的_________极,理由是________________________________。
(1)MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)能
(3)防止发生副反应,生成NaClO3
(4)2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑ 2NaOH+Cl2====NaClO+NaCl+H2O(或NaCl+H2O
2NaOH+H2↑+Cl2↑ 2NaOH+Cl2====NaClO+NaCl+H2O(或NaCl+H2O![]() NaClO+H2↑)
NaClO+H2↑)
(5)正 使生成的Cl2充分与阴极生成的NaOH反应,并防止Cl2从上部的导管逸出污染环境
解析:(2)去掉“浓硫酸”仍能达到目的,“浓硫酸”是干燥剂,但后面的反应与“干燥”无关。
(5)既然装置B是用来制取NaClO而不是制Cl2,所以要尽可能长时间地让Cl2留在溶液中(与NaOH反应),所以应从下面的极产生。

练习册系列答案
相关题目