题目内容
【题目】化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,下列叙述正确的是
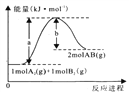
A. 每生成2个AB分子放出bkJ热量
B. AB(g) =![]() A2(g)+
A2(g)+ ![]() B2(g) △H=-
B2(g) △H=-![]() (a-b)kJ·mol-l
(a-b)kJ·mol-l
C. 该反应中生成物的总能量低于反应物的总能量
D. 断裂1 mol A2和1 mol B2中的化学键,放出a kJ能量
【答案】B
【解析】A. 根据图像可知反应物总能量低于生成物总能量,因此是吸热反应,A错误;B. 根据图像可知生成2molAB的反应热是(a-b)kJ·mol-l,所以AB(g) =![]() A2(g)+
A2(g)+ ![]() B2(g) △H=-
B2(g) △H=-![]() (a-b)kJ·mol-l,B正确;C. 该反应中生成物的总能量高于反应物的总能量,C错误;D. 断裂1 mol A2和1 mol B2中的化学键,吸收a kJ能量,D错误,答案选B。
(a-b)kJ·mol-l,B正确;C. 该反应中生成物的总能量高于反应物的总能量,C错误;D. 断裂1 mol A2和1 mol B2中的化学键,吸收a kJ能量,D错误,答案选B。

【题目】蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁的实验步骤如下图所示:
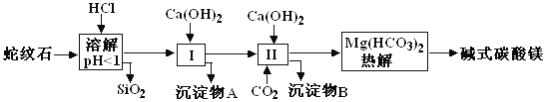
(1)蛇纹石加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是__________。
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见下表)。
氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 1.5 | 3.3 | 9.4 |
Ca(OH)2不能过量,若Ca(OH)2过量可能会导致__________溶解、________沉淀。
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入__________(填写物质的化学式),然后过滤、洗涤、灼烧。
(4)现设计一个实验,确定产品aMgCO3bMg(OH)2cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量 ②高温分解
③ ______________________________________________________。
④称量碱石灰吸收CO2前后的质量 ⑤MgO称量
(5)18.2 g产品完全分解后,产生6.6 g CO2和8.0 g MgO,由此可知,产品的化学式中:a=____________,b=____________,c=____________。