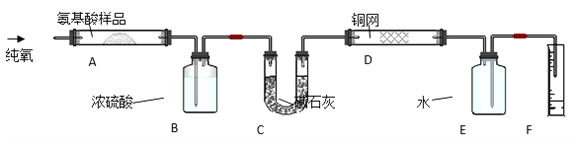
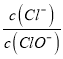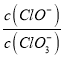题目内容
【题目】氟化钾是一种重要的无机氟化工产品,广泛应用于医药、农药和金属冶炼等领域。采用湿法磷酸副产物氟硅酸(![]() ,含有少量
,含有少量![]() 、
、![]() 等)制备氟化钾的工艺流程如图所示(已知:
等)制备氟化钾的工艺流程如图所示(已知:![]() ):
):
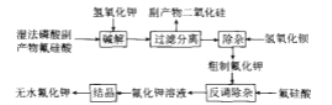
请回答下列问题:
(1)碱解过程主要反应的化学方程式为_____,其中要严格控制KOH用量,否则易生成副产物_____(填化学式)溶解在滤液中。
(2)碱解反应中温度对氟化钾收率的影响如图所示。由如图可知,实验选择适宜的反应温度为____;最高点后,随温度升高曲线下降的原因可能是_______。
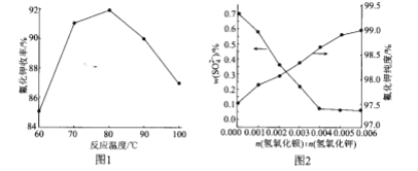
(3)Ba(OH)2加入量对![]() 含量和氟化钾纯度的影响如图所示。当
含量和氟化钾纯度的影响如图所示。当![]() 由0.004到0.005时,氟化钾的纯度升高,这是由于__。
由0.004到0.005时,氟化钾的纯度升高,这是由于__。
(4)Ba(OH)2和BaCO3是常见的除硫试剂。若使用BaCO3代替Ba(OH)2,当沉淀转化达到平衡时,滤液中![]() ___[已知
___[已知![]() ,
,![]() ,保留小数点后三位]。
,保留小数点后三位]。
(5)浓度均为0.1mol/L的KF和HF的混合溶液中:2c(H+)-2c(OH-)____c(F-)-c(HF) (填“>”“<”或“=”)。
(6)1986年,化学家Karl Chrite用KMnO4和KF、HF混合溶液反应生成稳定配离子![]() ,该反应氧化产物是一种常见的无色无味气体单质,则该反应的离子方程式为_____。
,该反应氧化产物是一种常见的无色无味气体单质,则该反应的离子方程式为_____。
【答案】![]()
![]() 80℃ 温度过高时,
80℃ 温度过高时,![]() 易分解为SiF4和HF 除硫过程中,Ba2+能与KF溶液中少量的
易分解为SiF4和HF 除硫过程中,Ba2+能与KF溶液中少量的![]() 反应生成沉淀 0.022 =
反应生成沉淀 0.022 = ![]()
【解析】
通过湿法磷酸副产物氟硅酸制备氟化钾的过程中,碱解过程主要发生的反应为氟硅酸与氢氧化钾的反应,生成二氧化硅及酸碱中和反应的盐![]() ,其中
,其中![]() 为目标产物,硅酸钾则为需要除去的杂质。为了减少
为目标产物,硅酸钾则为需要除去的杂质。为了减少![]() 的量,需要控制氢氧化钾的用量。通过过滤除去二氧化硅等不溶物,再加入氢氧化钡除去
的量,需要控制氢氧化钾的用量。通过过滤除去二氧化硅等不溶物,再加入氢氧化钡除去![]() 和少量的
和少量的![]() ,即可获得粗制的
,即可获得粗制的![]() ,据此答题。
,据此答题。
(1)碱解过程主要发生的反应为氟硅酸与氢氧化钾的反应,会生成二氧化硅及酸碱中和反应的盐![]() ,故该反应方程式可写为
,故该反应方程式可写为![]() 。该反应要严格控制KOH用量,否则易使
。该反应要严格控制KOH用量,否则易使![]() 溶解,产生更多的副产物
溶解,产生更多的副产物![]() ,故答案为
,故答案为![]() 、
、![]() ;
;
(2)从图中可知80℃时,氟化钾收率最高,故实验选择适宜的反应温度为80℃;但由于温度过高时,![]() 易分解为SiF4和HF,所以在80℃最高点后,随温度升高曲线下降,故答案应为80℃、温度过高时,
易分解为SiF4和HF,所以在80℃最高点后,随温度升高曲线下降,故答案应为80℃、温度过高时,![]() 易分解为SiF4和HF;
易分解为SiF4和HF;
(3)由于在除硫过程中,Ba2+能与KF溶液中少量的![]() 反应生成沉淀,所以当
反应生成沉淀,所以当![]() 由0.004到0.005时,氟化钾的纯度升高,故答案应为Ba2+能与KF溶液中少量的
由0.004到0.005时,氟化钾的纯度升高,故答案应为Ba2+能与KF溶液中少量的![]() 反应生成沉淀;
反应生成沉淀;
(4)Ba(OH)2和BaCO3是常见的除硫试剂。若使用BaCO3代替Ba(OH)2,当沉淀转化达到平衡时,滤液中![]() =
=![]() = 0.022,故答案应为0.022;
= 0.022,故答案应为0.022;
(5)浓度均为0.1mol/L的KF和HF的混合溶液中存在电荷守恒关系为: c(![]() )+ c(
)+ c(![]() ) =c(
) =c(![]() )+c(
)+c(![]() );物料守恒关系为:2c(
);物料守恒关系为:2c(![]() )= c(
)= c(![]() )+ c(HF) 。将物料守恒中c(
)+ c(HF) 。将物料守恒中c(![]() ) 代入电荷守恒中,即可得到2c(
) 代入电荷守恒中,即可得到2c(![]() )-2c(
)-2c(![]() )=c(
)=c(![]() )-c(HF),故答案为:=;
)-c(HF),故答案为:=;
(6)KMnO4和KF、HF混合溶液反应可生成稳定配离子![]() ,该反应氧化产物为氧气,则根据氧化还原反应对该反应的离子方程式进行配平为
,该反应氧化产物为氧气,则根据氧化还原反应对该反应的离子方程式进行配平为![]() ,故答案为
,故答案为![]()

【题目】硫酸铜是一种应用极其广泛的化工原料;以下是某工厂用含铁废铜为原料生产胆矾(CuSO45H2O)和副产物石膏(CaSO42H2O)的生产流程示意图:

胆矾和石膏在不同温度下的溶解度(g/100g水)见表。
温度(℃) | 20 | 40 | 60 | 80 | 100 |
石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
请回答下列问题:
(1)红棕色滤渣的主要成分是___;
(2)写出浸出过程中生成硫酸铜的离子方程式___;
(3)操作I包括蒸发浓缩、__等操作,温度应该控制在__℃左右;
(4)从溶液中分离出硫酸铜晶体的操作Ⅱ应为__、___、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是__;干燥时采用晾干,不用加热烘干的原因是___。
(5)取样检验是为了确认Fe3+是否除净。有同学设计了以下两种方案,在实验室分别对所取样品按下列方案进行操作:
方案一:取样于试管→滴加KSCN溶液; 方案二:纸层析→喷KSCN溶液;
①你认为上述两种方案设计更合理的是__;
②指出你认为不合理方案存在的问题是__。