题目内容
据材料称:钠可在氮气中燃烧生成氮化钠,氮化钠与水反应的化学方程式是:
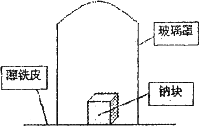
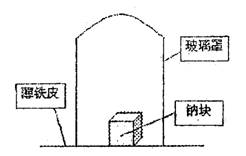
Na3N+4H2O=3NaOH+NH3?H2O。某学校化学研究学习小组,为了研究钠在空气中燃烧产物的成分,做了以下实验:取11.5g钠单质放在一块薄铁皮上,上扣一玻璃罩(玻璃罩内为干燥且无酸性气体的空气),用酒精灯加热薄铁皮,钠完全燃烧,将燃烧产物投入水中,得到一种纯净气体0.224L(标准状态)和1.00L溶液,从中取出25.0mL溶液,和13.5mL 1.00mol?L-1HC1溶液刚好完全反应。求钠在空气中燃烧产物的成分及物质的量。
解:n(Na)=0.500mol
钠在有限的空气中燃烧可能有Na2O、Na2O2、Na3N。
n(O2)=![]()
2Na2O2+2H2O=4NaOH+O2↑
0.0200mol 0.0100ml
n(Na2O2)=0.0200mol
Na→NaOH,由Na守恒知
c(NaOH)=0.0500mol?L-1,25mL溶液中n(NaOH)=1.25×10-2mol
n(HC1)=1.35×10-2mol>n(NaOH),说明溶液中还有氨水。
原1L溶液中n(NH3?H2O)=![]()
Na3N=4H2O=3NaOH+NH3?H2O
4.00×10-2mol 4.00×10-2mol
即:n(Na3N)=0.0400mol
n(Na2O)=(0.0500 mol-0.0400mol×3-0.0200mol×2)/2=0.170mol

练习册系列答案
相关题目