题目内容
2.用Pt电极电解含0.2mol CuSO4溶液一段时间后,阳极上生成4.48L气体(标准状况),为了恢复到电解前的状态,应加入( )| A. | CuO 16.0g | B. | Cu(OH)2 19.6g | C. | Cu 12.8g | D. | CuCO3 24.8g |
分析 阳极上OH-放电生成O2,n(O2)=$\frac{4.48L}{22.4L/mol}$=0.2mol,转移电子物质的量=0.2mol×4=0.8mol,如果Cu2+完全放电转移电子物质的量=0.2mol×2=0.4mol<0.8mol,所以阴极上H+还放电生成氢气,所以实质上相当于电解得到CuO和H2O,要是溶液恢复到原状态,需要加入CuO和H2O,电解生成n(H2)=$\frac{0.8mol-0.4mol}{2}$=0.2mol,所以氢气和Cu的物质的量相等,所以析出的相当于Cu(OH)2,根据Cu原子守恒计算加入固体质量.
解答 解:阳极上OH-放电生成O2,n(O2)=$\frac{4.48L}{22.4L/mol}$=0.2mol,转移电子物质的量=0.2mol×4=0.8mol,如果Cu2+完全放电转移电子物质的量=0.2mol×2=0.4mol<0.8mol,所以阴极上H+还放电生成氢气,所以实质上相当于电解得到CuO和H2O,要是溶液恢复到原状态,需要加入CuO和H2O,电解生成n(H2)=$\frac{0.8mol-0.4mol}{2}$=0.2mol,所以氢气和Cu的物质的量相等,所以析出的相当于Cu(OH)2,根据Cu原子守恒=0.2mol×98g/mol=19.6g,故选B.
点评 本题考查电解原理,正确判断阴极上析出物质成分是解本题关键,利用转移电子守恒进行计算即可,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.下列措施有利于节能减排、保护环境的是:①加快化石燃料的开采与使用;②研发易降解
的生物农药;③应用高效洁净的能源;④田间焚烧秸秆;⑤推广使用节能环保材料.( )
的生物农药;③应用高效洁净的能源;④田间焚烧秸秆;⑤推广使用节能环保材料.( )
| A. | ①③⑤ | B. | ②③⑤ | C. | ①②④ | D. | ②④⑤ |
10.下列物质中既含有非极性键,又含有极性键的是( )
| A. | CH4 | B. | Na2O2 | C. | C2H5OH | D. | H2O |
17.乙烯酮(CH2=C=O)在一定条件下,能与含活泼氢的化合物发生如下反应,其反应可表示为:CH2=C=O+HA→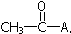 .下列各试剂,在一定条件下与乙烯酮发生反应,其产物不正确的是( )
.下列各试剂,在一定条件下与乙烯酮发生反应,其产物不正确的是( )
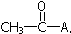 .下列各试剂,在一定条件下与乙烯酮发生反应,其产物不正确的是( )
.下列各试剂,在一定条件下与乙烯酮发生反应,其产物不正确的是( )| A. | HCl与之加成,生成CH3COCl | B. | CH3OH与之加成,生成CH3COCH2OH | ||
| C. | H2O与之加成,生成CH3COOH | D. | CH3COOH与之加成,生成 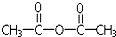 |
7.设NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 1mol Na2O2 中有4 NA个离子 | |
| B. | 常温常压下,11.2L氧气所含的原子数为NA | |
| C. | 1L 1mol/L CH3COONa溶液中含NA个CH3COO-离子 | |
| D. | 42g C2H4和C3H6的混合物中一定含有6NA个氢原子 |
11.下列有关有机物同分异构体说法中不正确的是( )
| A. | 分子式为C4H8的同分异构体共有(不考虑立体异构)5种 | |
| B. | 立方烷(C8H8)的六氯取代物有3种 | |
| C. | 分子式为C5H10O2的同分异构体中属于酯的有8种 | |
| D. | CH3 OCH3的一溴取代物有4种 OCH3的一溴取代物有4种 |
12.下列化学术语或表示方法错误的是( )
| A. | S2-的结构示意图: | B. | CO2的结构式:O=C=O | ||
| C. | 醋酸的分子式:CH3COOH | D. | 乙烯的结构简式:CH2=CH2 |