题目内容
实验室中配制碘水,往往是将I2溶于KI溶液中,这样就可以得到浓度较大的碘水,主要是因为发生了反应:I2(aq)+I-![]() I3-上述平衡体系中,I3-的物质的量浓度c(I3-)与温度T的关系如下图所示(曲线上的任何一点都表示平衡状态).
I3-上述平衡体系中,I3-的物质的量浓度c(I3-)与温度T的关系如下图所示(曲线上的任何一点都表示平衡状态).
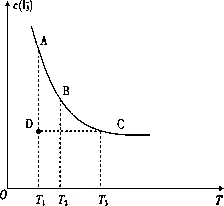
(1)通过分析上图,该反应的正反应为________反应(填吸热或放热),
(2)A状态与C状态的化学反应速率比较为v(A)________v(C)(填>、<或=).
(3)在T1、D状态时,v正________v逆(填>、<或=).
答案:
解析:
解析:
(1)放热(1分)
(2)<(1分)
(3)>(1分)

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
文献资料显示某地区的酸雨主要为硫酸型和盐酸型酸雨.某兴趣小组对酸雨进行实验研究.
(1)提出合理的假设:该酸雨中的溶质除H2SO4、HC1外,该小组同学根据硫酸型酸雨的形成过程,预测主要溶质还一定有 .
(2)设计实验方案验证以上假设.在答题卡上写出实验步骤、预期现象和结论.限选试剂及仪器:盐酸、硝酸、BaC12溶液、Ba(OH)2溶液、AgNO3溶液、紫色石蕊试液、品红溶液、烧杯、试管、胶头滴管.
(3)酸雨部分组成测定:
①标准溶液配制:实验室用1.000mol?L-1较浓的碘水配制250mL 0.02000mol?L-1的碘水溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需 .
②滴定:准确量取25.00mL该酸雨于锥形瓶中,加入几滴 溶液作指示剂,将0.02000mol?L-1碘水装入50mL酸式滴定管,滴定终点现象为 ,记录数据,重复滴定2次,平均消耗碘水VmL.
计算:被碘水氧化的物质的量浓度之和为 (只列出算式,不做运算)
(1)提出合理的假设:该酸雨中的溶质除H2SO4、HC1外,该小组同学根据硫酸型酸雨的形成过程,预测主要溶质还一定有
(2)设计实验方案验证以上假设.在答题卡上写出实验步骤、预期现象和结论.限选试剂及仪器:盐酸、硝酸、BaC12溶液、Ba(OH)2溶液、AgNO3溶液、紫色石蕊试液、品红溶液、烧杯、试管、胶头滴管.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量酸雨于A、B两支洁净试管中,待用 | 无明显现象 |
| 步骤2:往A试管中加入过量的Ba(OH)2溶液,静置,过滤 | 有白色沉淀 |
| 步骤3:取少量步骤2得到的滤渣加入过量盐酸 | 滤渣不能完全溶解,说明酸雨中含有硫酸 |
| 步骤4:取适量步骤2得到的滤液, |
|
| 步骤5:往B试管中加入 |
①标准溶液配制:实验室用1.000mol?L-1较浓的碘水配制250mL 0.02000mol?L-1的碘水溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需
②滴定:准确量取25.00mL该酸雨于锥形瓶中,加入几滴
计算:被碘水氧化的物质的量浓度之和为
 灼烧
灼烧