题目内容
下图所示的装置中,容器甲内充入0.1mol NO气体,干燥管内装有一定量的Na2O2,从A处缓慢通入CO2气体。恒温下,容器甲中活塞缓慢由B向左移动,当移至C处时,容器体积缩小至最小,为原体积的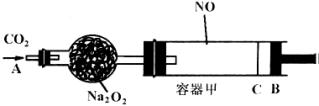
(1)①已知当活塞移至C处时,干燥管中物质的质量增加了2.24g。此时,通入标准状况下的CO2气体多少L?容器甲中NO2转化为N2O4的转化率是多少?
②活塞移至C处后,继续通入amol CO2,此时活塞恰好回至B处。则a值必小于0.0l,其理由是____ _____。
(2)若改变干燥管中Na2O2的量,可通过调节甲容器的温度及通入CO2的量,使活塞发生从B到C,又从C到B的移动。则Na2O2的质量最小值应大于_________g。
答案:
解析:
提示:
解析:
| (1)①1.792;a=25% ②当活塞由C向B移动时,因体积扩大,使平衡2NO2 (2)1.56
|
提示:
| 建议用差量法进行计算。
|

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
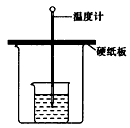
50ml0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。
回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器
是 。装置中还存在的2个错误是①__
② 这种错误会造成最高温度读数________(填“增大”、“减小”或“无影响”);测得的中和热将____________(填“偏大”、“偏小”或“无影响”)。
(2)在实验过程中,该同学需要测定并记录的实验数据有 (填序号)。
| A.盐酸的浓度 |
| B.盐酸的温度 |
| C.氢氧化钠溶液的浓度 |
| D.氢氧化钠溶液的温度 |
F.反应后混合溶液的终止温度
(3)实验中改用60mL0.50mol·L-1盐酸跟50mL0.55mol·L-1NaOH溶液进行反应,与上述正确的实验操作相比,所放出的热量 (填“相等”或“不相等”),所求中和热 (填“相等”或“不相等”)。
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会 ;(填“偏大”“偏小”或“无影响”)。