题目内容
在标准状况下,与12g H2的体积相等的N2的
- A.质量为12g
- B.物质的量为6mol
- C.体积为22.4L/mol
- D.物质的量为12mol
B
分析:标准状况下Vm=22.4L/mol,n(H2)=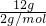 =6mol,根据V=n?Vm可知,同温同压下,相同物质的量的气体的体积相同,以此解答该题.
=6mol,根据V=n?Vm可知,同温同压下,相同物质的量的气体的体积相同,以此解答该题.
解答:标准状况下Vm=22.4L/mol,n(H2)=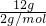 =6mol,则
=6mol,则
A.n(N2)=6mol,m(N2)=6mol×28g/mol=168g,故A错误;
B.根据V=n?Vm可知,同温同压下,相同物质的量的气体的体积相同,在标准状况下,与12g H2的体积相等的N2的物质的量为6mol,故B正确;
C.n(N2)=6mol,则V(N2)=6mol×22.4L/mol=134.4L,故C错误;
D.标准状况下,氢气与氮气的体积相同,则物质的量相同,即n(N2)=n(H2)=6mol,故D错误.
故选B.
点评:本题考查阿伏加德罗定律及其推论,题目难度不大,本题注意相关计算公式的运用.
分析:标准状况下Vm=22.4L/mol,n(H2)=
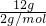 =6mol,根据V=n?Vm可知,同温同压下,相同物质的量的气体的体积相同,以此解答该题.
=6mol,根据V=n?Vm可知,同温同压下,相同物质的量的气体的体积相同,以此解答该题.解答:标准状况下Vm=22.4L/mol,n(H2)=
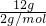 =6mol,则
=6mol,则A.n(N2)=6mol,m(N2)=6mol×28g/mol=168g,故A错误;
B.根据V=n?Vm可知,同温同压下,相同物质的量的气体的体积相同,在标准状况下,与12g H2的体积相等的N2的物质的量为6mol,故B正确;
C.n(N2)=6mol,则V(N2)=6mol×22.4L/mol=134.4L,故C错误;
D.标准状况下,氢气与氮气的体积相同,则物质的量相同,即n(N2)=n(H2)=6mol,故D错误.
故选B.
点评:本题考查阿伏加德罗定律及其推论,题目难度不大,本题注意相关计算公式的运用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目