题目内容
【题目】常温下,将![]() 缓慢通入水中至饱和,然后向其中滴加
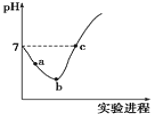
缓慢通入水中至饱和,然后向其中滴加![]() 溶液。整个实验过程中溶液的pH变化曲线如图所示,不考虑次氯酸分解,下列叙述正确的是
溶液。整个实验过程中溶液的pH变化曲线如图所示,不考虑次氯酸分解,下列叙述正确的是![]()
![]()
A.![]() 段,溶液中
段,溶液中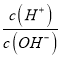 减小
减小
B.c点对应溶液中:![]()
C.b点对应溶液中:![]()
D.实验过程中用pH试纸测定溶液的pH
【答案】B
【解析】
A.由a点到b点的过程是氯气的溶解平衡![]() 向右进行的过程,酸性逐渐增强,氢离子浓度逐渐增大,溶液中
向右进行的过程,酸性逐渐增强,氢离子浓度逐渐增大,溶液中![]()
![]()
![]() 增大,选项A错误;
增大,选项A错误;
B.c点溶液呈中性,则![]() ,根据电荷守恒得
,根据电荷守恒得![]() ,所以
,所以![]() ,选项B正确;
,选项B正确;
C.b点所示溶液中发生反应:![]() ,HClO为弱电解质,部分电离,溶液中存在的粒子有:
,HClO为弱电解质,部分电离,溶液中存在的粒子有:![]() 、
、![]() 、
、![]() 、
、![]() ,
,![]() 、HClO、
、HClO、![]() ,溶液中:
,溶液中:![]() ,选项C错误;
,选项C错误;
D.溶液中含有次氯酸,具有漂白性,不能用pH试纸测pH,应选pH计,选项D错误;
答案选B。

【题目】氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用。
(1)根据下列能量变化示意图,请写出![]() 和CO反应的热化学方程式______。
和CO反应的热化学方程式______。

(2)在固定体积的密闭容器中,进行如下化学反应: ![]()
![]() H<0,其平衡常数K与温度T的关系如下表:
H<0,其平衡常数K与温度T的关系如下表:
T/K | 298 | 398 | 498 |
平衡常数K |
|
|
|
①试判断![]() ______
______![]() (填写>、=,<)
(填写>、=,<)
②下列各项能说明该反应已达到平衡状态的是_______(填字母)
a. 容器内![]() 、
、![]() 、
、![]() 的浓度之比为1:3:2
的浓度之比为1:3:2
b. ![]()
c. 容器内压强保持不变
d. 混合气体的密度保持不变
(3)对反应![]()
![]() H>0,在温度分别为
H>0,在温度分别为![]() 、
、![]() 时,平衡体系中
时,平衡体系中![]() 的体积分数随压强变化曲线如下图所示。
的体积分数随压强变化曲线如下图所示。

①A、C两点的反应速率:A_________C(填>、=、<)
②A、C两点![]() 的转化率:A_________C(填>、=、<)
的转化率:A_________C(填>、=、<)
③由状态B到状态A,可以采用的方法是__________。
(4)一定温度下
①若在1L的密闭容器中,充入1 mol![]() 和3 mol
和3 mol![]() 发生反应,并维持容积恒定,10min达到平衡时,气体的总物质的量为原来的7/8,则
发生反应,并维持容积恒定,10min达到平衡时,气体的总物质的量为原来的7/8,则![]() 的转化率a(
的转化率a(![]() )=______,以
)=______,以![]() 表示该过程的反应速率v(
表示该过程的反应速率v(![]() )=_________.
)=_________.
②若在1L的密闭容器中,充入2mol![]() 和6mol
和6mol![]() 发生反应,并维持压强恒定,达到平衡时,
发生反应,并维持压强恒定,达到平衡时, ![]() 平衡浓度比①中
平衡浓度比①中![]() 平衡浓度的2倍________。(填>、=、<)
平衡浓度的2倍________。(填>、=、<)