题目内容
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤
正确的操作顺序是
| A.③②①⑤④ | B.①②③⑤④ | C.②③①④⑤ | D.③⑤②①④ |
A
解析试题分析:Na2CO3溶液的作用为除去食盐水中的Ca2+和除去过量的BaCl2,所以Na2CO3溶液要在BaCl2溶液之后,NaOH溶液的顺序可在BaCl2、Na2CO3之前、中间或后面,然后过滤,在滤液中加入稀盐酸,除去过量的NaOH、Na2CO3,故A项正确。
考点:本题考查食盐水的提纯。

练习册系列答案
相关题目
为了除去粗盐中的Ca2+、Mg2+、SO42—及泥沙,可将粗盐溶于水,然后进行下列五项操作,其中正确的操作顺序是( )
①过滤 ②加过量的NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液
| A.①④②⑤③ | B.④①②⑤③ | C.④②①③⑤ | D.⑤②④①③ |
某固体NaOH因吸收了空气中的CO2而含有杂质,若要将该固体配制成较纯的溶液,则其主要的实验操作过程应是
| A.溶解→加适量BaCl2溶液→过滤 | B.溶解→加适量CaCl2溶液→过滤 |
| C.溶解→加适量Ca(OH)2溶液→过滤 | D.溶解→加适量盐酸→加热 |
如图,在盛有碘水的三支试管中分别加入苯(密度比水小,不溶于水)、四氯化碳和酒精,振荡后静置,出现下列现象,正确的结论有( )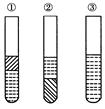
| A.①加入的是CCl4,②是苯,③加酒精 |
| B.①加入的是酒精,②加CCl4,③加苯 |
| C.①加入的是苯,②加CCl4,③加酒精 |
| D.①加入的是苯,②加酒精,③加CCl4 |
已知甲和乙的某些性质如下表所示:
| 物质 | 熔点(℃) | 沸点(℃) | 密度(g·mL-1) | 在水中的溶解性 |
| 甲 | -98 | 37. 5 | 0.93 | 可溶 |
| 乙 | -48 | 95 | 0.90 | 可溶 |
现有甲和乙的混合物,进行分离时,可采用的方法是( )
A.蒸馏 B.蒸发 C.过滤 D.萃取
已知丙酮通常是无色的液体,与水互溶,密度小于1 g/mL ,沸点约为55℃。要将水与丙酮分离出来,选择的方法是( )
| A.蒸馏 | B.分液 | C.过滤 | D.蒸发 |
海水晒盐的原理( )
| A.利用热蒸发浓缩海水达饱和并进一步结晶 |
| B.通过降温降低食盐的溶解度使食盐析出 |
| C.利用加入沉淀剂的方法是食盐沉淀析出 |
| D.利用泥沙使海水达到饱和,然后利用日光使食盐析出 |
下列除去杂质的方法正确的是
| A.除去CO2中混有的CO:用澄清石灰水洗气 |
| B.除去BaCO3固体中混有的BaSO4:加过量盐酸后,过滤、洗涤 |
| C.除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤 |
| D.除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤 |