题目内容
饮用水中NO- 3 |
- 3 |
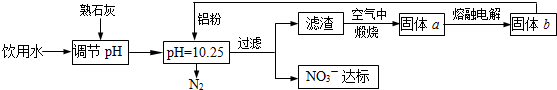
请回答下列问题:
(1)该方案中选用熟石灰调节pH,理由是
(2)已知过滤后得到的滤渣是Al和Al(OH)3,则在溶液中铝粉和NO
- 3 |
(3)用H2催化还原法也可降低饮用水中NO
- 3 |
(4)饮用水中的NO
- 3 |
+ 4 |
+ 4 |
- 3 |
+ 4 |
- 3 |
分析:(1)铝粉与硝酸根离子发生氧化还原反应生成固体,则固体为氢氧化铝,则硝酸被还原为氮气;
(2)选用熟石灰调节pH,原料来源丰富,价格便宜,且引人离子对人体无害,注意pH过大或过小,都将直接发生Al与酸或碱的反应;
(3)用H2催化还原法也可降低饮用水中NO3-的浓度,反应中的还原产物和氧化产物均可参与大气循环,则产物为水和氮气;
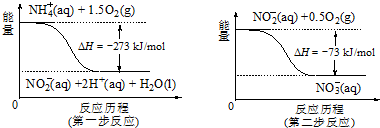
(4)由图可知,第一步热化学反应为NH4+ (aq)+1.5O2(g)=2H+(aq)+NO2- (aq)+H2O(l)△H=-2736 kJ?mol-1,第二步热化学反应为NO2- (aq)+0.5O2(g)=NO3- (aq))△H=-73kJ?mol-1,利用盖斯定律可计算1mol NH4+(aq)全部氧化成NO3- (aq)的热化学方程式.
(2)选用熟石灰调节pH,原料来源丰富,价格便宜,且引人离子对人体无害,注意pH过大或过小,都将直接发生Al与酸或碱的反应;
(3)用H2催化还原法也可降低饮用水中NO3-的浓度,反应中的还原产物和氧化产物均可参与大气循环,则产物为水和氮气;
(4)由图可知,第一步热化学反应为NH4+ (aq)+1.5O2(g)=2H+(aq)+NO2- (aq)+H2O(l)△H=-2736 kJ?mol-1,第二步热化学反应为NO2- (aq)+0.5O2(g)=NO3- (aq))△H=-73kJ?mol-1,利用盖斯定律可计算1mol NH4+(aq)全部氧化成NO3- (aq)的热化学方程式.
解答:解:(1)选用熟石灰调节pH,原料来源丰富,价格便宜,且引人离子对人体无害,注意pH过大或过小,都将直接发生Al与酸或碱的反应,否则会造成Al的大量消耗,
故答案为:来源丰富、价格便宜;引入的Ca2+对人体无害;铝;
(2)铝粉与硝酸根离子发生氧化还原反应生成固体,则固体为氢氧化铝,则硝酸被还原为氮气,则在溶液中铝粉和NO3-反应的离子方程式为10Al+6NO3-+18H2O=10Al(OH)3+3N2↑+6OH-,
故答案为:10Al+6NO3-+18H2O=10Al(OH)3+3N2↑+6OH-;
(3)H2催化还原饮用水中NO3-,反应中的还原产物和氧化产物均可参与大气循环,则产物为水和氮气,该反应为5H2+2NO3-
N2+4H2O+2OH-(或5H2+2NO3-+2H+
N2↑+6H2O).
故答案为:5H2+2NO3-
N2+4H2O+2OH-(或5H2+2NO3-+2H+
N2↑+6H2O)
(4)由图可知,第一步热化学反应为NH4+ (aq)+1.5O2(g)=2H+(aq)+NO2- (aq)+H2O(l)△H=-2736 kJ?mol-1①,
第二步热化学反应为NO2- (aq)+0.5O2(g)=NO3- (aq))△H=-73kJ?mol-1②,
由盖斯定律可知①+②得1mol NH4+(aq)全部氧化成NO3- (aq)的热化学方程式为NH4+ (aq)+2O2(g)=2H+(aq)+NO3- (aq)+H2O(l)△H=-346 kJ?mol-1,
故答案为:NH4+ (aq)+2O2(g)=2H+(aq)+NO3- (aq)+H2O(l)△H=-346 kJ?mol-1.
故答案为:来源丰富、价格便宜;引入的Ca2+对人体无害;铝;
(2)铝粉与硝酸根离子发生氧化还原反应生成固体,则固体为氢氧化铝,则硝酸被还原为氮气,则在溶液中铝粉和NO3-反应的离子方程式为10Al+6NO3-+18H2O=10Al(OH)3+3N2↑+6OH-,
故答案为:10Al+6NO3-+18H2O=10Al(OH)3+3N2↑+6OH-;
(3)H2催化还原饮用水中NO3-,反应中的还原产物和氧化产物均可参与大气循环,则产物为水和氮气,该反应为5H2+2NO3-
| ||
| ||
故答案为:5H2+2NO3-
| ||
| ||
(4)由图可知,第一步热化学反应为NH4+ (aq)+1.5O2(g)=2H+(aq)+NO2- (aq)+H2O(l)△H=-2736 kJ?mol-1①,
第二步热化学反应为NO2- (aq)+0.5O2(g)=NO3- (aq))△H=-73kJ?mol-1②,
由盖斯定律可知①+②得1mol NH4+(aq)全部氧化成NO3- (aq)的热化学方程式为NH4+ (aq)+2O2(g)=2H+(aq)+NO3- (aq)+H2O(l)△H=-346 kJ?mol-1,
故答案为:NH4+ (aq)+2O2(g)=2H+(aq)+NO3- (aq)+H2O(l)△H=-346 kJ?mol-1.
点评:本题以信息的形式考查氧化还原反应、离子反应及热化学反应,注重对化学用语的考查,注意知识与题目信息的结合来解答,对学生能力要求较高,题目难度中等.

练习册系列答案
相关题目
