题目内容
【题目】ClO2是新一代饮用水的消毒剂,许多发达国家的自来水厂采用ClO2代替Cl2来进行自来水消毒.我国最近成功研制出制取ClO2的新方法,其反应的微观过程如下所示: 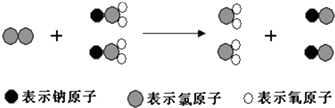
下列有关该反应的叙述中正确的是( )
A.该反应的化学方程式为Cl2+2NaClO2═2ClO2+2NaCl
B.该反应是应是复分解反应
C.反应中Cl2既是氧化剂,又是还原剂
D.NaClO2和ClO2中Cl元素的化合价相同
【答案】A
【解析】解:A.由三种小球表示的原子及微观过程可知,反应物为氯气和NaClO2 , 生成物为ClO2和NaCl,则反应为Cl2+2NaClO2═2ClO2+2NaCl,故A正确;
B.由不同的小球代表的原子可知,反应物为氯气和NaClO2 , 氯气为单质,则该反应一定不是复分解反应,故B错误;
C.Cl2+2NaClO2═2ClO2+2NaCl,反应中氯气中 的氯元素化合价0价变化为﹣1价,NaClO2中氯元素化合价+3价升高到+4价,所以氯气做氧化剂,故C错误;
D.根据化合价规则,NaClO2和ClO2中Cl的化合价分别是+3价和+4价,化合价不一样,故D错误;
故选A.
A.由不同小球代表的原子及反应的微观过程来分析,书写反应方程式;
B.复分解反应是化合物与化合物反应生成化合物与化合物的反应;
C.依据化学方程式中氯元素化合价的变化判断,氯气中 氯元素化合价0价变化为﹣1价;
D.根据化合物中元素化合价代数和为0计算来确定元素的化合价.

 阅读快车系列答案
阅读快车系列答案【题目】某地环保部门取一定量某工厂所排废水试样分成甲、乙、丙、丁四份,进行如图所示探究。
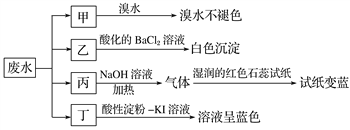
已知废水试样中可能含有下表中的离子:
离子 | |
阳离子 | Na+、Mg2+、X |
阴离子 | Cl-、SO |
请回答下列问题:
(1)离子X是______________(填化学式,下同),离子Y是__________________。
(2)表中不能确定是否存在的阴离子是__________。
(3)写出废水试样中滴加酸性淀粉KI溶液所发生反应的离子方程式: ___________________。