题目内容
用活性炭还原法可以处理氮氧化物.某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g)═N2(g)+CO2(g)+Q kJ?mol-1.
在T1℃时,反应进行到不同时间测得各物质的浓度如下:
①T1℃时,该反应的平衡常数K= ;
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是 (填字母编号).
a.加入一定量的活性炭 b.通人一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则Q 0(填“>”或“<”).
在T1℃时,反应进行到不同时间测得各物质的浓度如下:
| 时间(Min) 浓度(mol?L-1) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是
a.加入一定量的活性炭 b.通人一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则Q
考点:化学平衡的影响因素
专题:化学平衡专题
分析:①依据图表数据分析平衡状态平衡浓度,20℃平衡浓度c(NO)=0.40mol/L,c(N2)=0.3mol/L,c(CO2)=0.30mol/L,结合平衡常数概念计算;
②反应前后是气体体积不变的反应,图表数据分析可知一氧化氮,氮气,二氧化碳浓度都增大,说明改变的条件是缩小体积增大浓度,或加入一氧化氮达到新平衡后个物质浓度增大;
③根据浓度比值的变化来确定移动方向.
②反应前后是气体体积不变的反应,图表数据分析可知一氧化氮,氮气,二氧化碳浓度都增大,说明改变的条件是缩小体积增大浓度,或加入一氧化氮达到新平衡后个物质浓度增大;
③根据浓度比值的变化来确定移动方向.
解答:
解:①20℃反应达到平衡状态,平衡浓度c(NO)=0.40mol/L,c(N2)=0.3mol/L,c(CO2)=0.30mol/L,C(s)+2NO(g)═N2(g)+CO2(g),平衡常数K=
=
;
故答案为:
;
②30min后,只改变某一条件,反应重新达到平衡,图表数据分析可知一氧化氮,氮气,二氧化碳浓度都增大;
a.加入一定量的活性炭是固体,对平衡无影响,故a不符合;
b.通入一定量的NO,反应正向进行,达到平衡后一氧化氮、氮气、二氧化碳浓度增大,故b符合;
c.适当缩小容器的体积,反应前后是气体体积不变的反应,平衡不动,但个物质浓度增大,符合要求,故c符合;
d.加入合适的催化剂,只能改变化学反应速率,不能改变平衡,浓度不变,故d不符合;
故答案为:bc;
③30min时,容器中NO、N2、CO2的浓度之比=0.040:0.030:0.030=4:3:3,30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则平衡向逆反应方向移动,所以逆反应是吸热反应,正反应是放热反应,则Q<0,故答案为:<.
| 0.30×0.30 |
| 0.402 |
| 9 |
| 16 |
故答案为:
| 9 |
| 16 |
②30min后,只改变某一条件,反应重新达到平衡,图表数据分析可知一氧化氮,氮气,二氧化碳浓度都增大;
a.加入一定量的活性炭是固体,对平衡无影响,故a不符合;
b.通入一定量的NO,反应正向进行,达到平衡后一氧化氮、氮气、二氧化碳浓度增大,故b符合;
c.适当缩小容器的体积,反应前后是气体体积不变的反应,平衡不动,但个物质浓度增大,符合要求,故c符合;
d.加入合适的催化剂,只能改变化学反应速率,不能改变平衡,浓度不变,故d不符合;
故答案为:bc;
③30min时,容器中NO、N2、CO2的浓度之比=0.040:0.030:0.030=4:3:3,30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则平衡向逆反应方向移动,所以逆反应是吸热反应,正反应是放热反应,则Q<0,故答案为:<.
点评:本题考查了化学平衡常数、化学平衡移动的影响因素等,侧重考查学生对数据的分析处理,题目难度中等.

练习册系列答案
相关题目
下列图示说法中正确的是( )
A、 |
B、 |
C、 |
D、 |
下列生活中涉及到的化学问题,说法不正确的是( )
| A、对病人进行“血液透析”,利用了胶体的性质 |
| B、食用含碘盐与淀粉溶液会变蓝 |
| C、利用粮食酿酒经过了淀粉→葡萄糖→乙醇等让化学变化过程 |
| D、竹炭具有超强的吸附能力,能批复新装修房屋内的有害气体 |
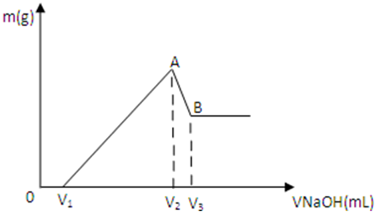 将0.1mol Mg、Al混合物溶于100mL 3mol/L HCl中,再滴加1mol/L NaOH溶液,在滴加NaOH溶液的过程中,沉淀的质量m随NaOH溶液体积V变化如图所示:
将0.1mol Mg、Al混合物溶于100mL 3mol/L HCl中,再滴加1mol/L NaOH溶液,在滴加NaOH溶液的过程中,沉淀的质量m随NaOH溶液体积V变化如图所示:
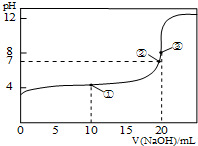 已知醋酸是日常生活中常见的弱酸.
已知醋酸是日常生活中常见的弱酸.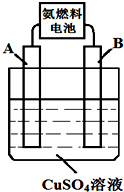 以氨气代替氢气研发氨燃料电池是当前科研的一个热点.
以氨气代替氢气研发氨燃料电池是当前科研的一个热点.