题目内容
【题目】下列说法中正确的是( )
A.氯化钠水溶液在电流的作用下电离出Na+和Cl-
B.硫酸钡难溶于水,但硫酸钡属于强电解质
C.二氧化碳溶于水能部分电离,故二氧化碳属于弱电解质
D.硫酸钠在水中的电离方程式可表示为Na2SO4=2Na++S6++4O2-
【答案】B
【解析】氯化钠在溶于水时即能电离出Na+和Cl,电解质的电离无需外加电流的作用,选项A不符合题意;
硫酸钡虽难溶于水,但硫酸钡溶于水的部分是完全电离的,因此硫酸钡属于强电解质,选项B符合题意;
二氧化碳溶于水生成的碳酸能部分电离,碳酸是弱电解质,而二氧化碳是非电解质,选项C不符合题意;
硫酸钠在水中的电离方程式应为Na2SO4=2Na++ ![]() ,选项D不符合题意。
,选项D不符合题意。
所以答案是:B
【考点精析】本题主要考查了强电解质和弱电解质的概念和判断的相关知识点,需要掌握强电解质:离子键、强极性键、完全电离;弱电解质:极性键、部分电离才能正确解答此题.

练习册系列答案
相关题目
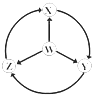
【题目】如图W、X、Y、Z为四种物质,若箭头表示能一步转化的常见反应,其中常温下能实现图示转化关系的是( )
选项 | W | X | Y | Z |
|
A | S | SO2 | SO3 | H2SO4 | |
B | Na | Na2O2 | NaOH | NaCl | |
C | Fe | FeCl3 | Fe(OH)2 | FeCl2 | |
D | Al | AlCl3 | NaAlO2 | Al2(SO4)3 |
A.A
B.B
C.C
D.D