题目内容
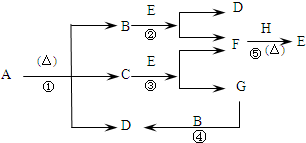
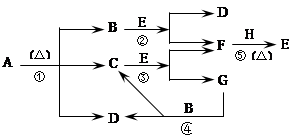
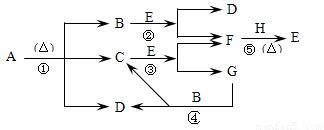
已知化合物A、D、E、G焰色反应时,火焰均呈黄色,其中A可用作家庭食品添加剂,也可用以治疗胃酸过多.A~H各物质的变化关系如图所示:
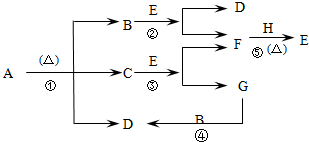
(1)写出下列反应的化学方程式,属于离子反应的,只写出离子方程式.
反应③
反应④
反应⑤
(2)上述三个反应中属于氧化还原反应的有

(1)写出下列反应的化学方程式,属于离子反应的,只写出离子方程式.
反应③
2Na2O2+2H2O═4Na++4OH-+O2↑
2Na2O2+2H2O═4Na++4OH-+O2↑
;反应④
2OH-+CO2═CO32-+H2O
2OH-+CO2═CO32-+H2O
;反应⑤
2Na+O2
Na2O2
| ||
2Na+O2
Na2O2
.
| ||
(2)上述三个反应中属于氧化还原反应的有
③⑤
③⑤
(填序号).分析:化合物A、D、E、G焰色反应时,火焰均呈黄色,说明是钠的化合物,其中A可用作家庭食品添加剂,也可用以治疗胃酸过多,判断A为NaHCO3,加热分解生成碳酸钠、二氧化碳、水,依据焰色反应可知,D为Na2CO3,E和B反应生成D和F,说明E为Na2O2,B为CO2,F为O2,H为Na;所以判断C为H2O,G为NaOH,依据判断出的物质分析回答问题.
解答:解:已知化合物A、D、E、G焰色反应时,火焰均呈黄色,说明是钠的化合物,其中A可用作家庭食品添加剂,也可用以治疗胃酸过多,判断A为NaHCO3,加热分解生成碳酸钠、二氧化碳、水,依据焰色反应可知,D为Na2CO3,E和B反应生成D和F,说明E为Na2O2,B为CO2,F为O2,H为Na;所以判断C为H2O,G为NaOH;
(1)反应③是过氧化钠和水的反应,反应的离子方程式为:2Na2O2+2H2O═4Na++4OH-+O2↑;
反应④是二氧化碳和氢氧化钠的反应,离子方程式为:2OH-+CO2═CO3 2-+H2O;
反应⑤是金属钠在氧气中的燃烧生成过氧化钠,反应的化学方程式为:2Na+O2
Na2O2,
故答案为:2Na2O2+2H2O═4Na++4OH-+O2↑;2OH-+CO2═CO32-+H2O;2Na+O2
Na2O2;
(2)上述三个反应中属于氧化还原反应的有:③⑤,故答案为:③⑤.
(1)反应③是过氧化钠和水的反应,反应的离子方程式为:2Na2O2+2H2O═4Na++4OH-+O2↑;
反应④是二氧化碳和氢氧化钠的反应,离子方程式为:2OH-+CO2═CO3 2-+H2O;
反应⑤是金属钠在氧气中的燃烧生成过氧化钠,反应的化学方程式为:2Na+O2
| ||
故答案为:2Na2O2+2H2O═4Na++4OH-+O2↑;2OH-+CO2═CO32-+H2O;2Na+O2
| ||
(2)上述三个反应中属于氧化还原反应的有:③⑤,故答案为:③⑤.
点评:本题考查了物质转化的应用,物质性质的分析判断,主要考查钠及其化合物性质的应用,离子方程式的书写和判断,氧化还原反应的判断方法,题目较简单.

练习册系列答案
相关题目
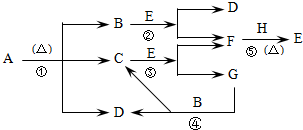 已知化合物A、D、E、G焰色反应时,火焰均呈黄色,其中A可用作家庭食品添加剂,也可用以治疗胃酸过多.A~H各物质的变化关系如图所示.
已知化合物A、D、E、G焰色反应时,火焰均呈黄色,其中A可用作家庭食品添加剂,也可用以治疗胃酸过多.A~H各物质的变化关系如图所示.