题目内容
(6分)向20mL某物质的量浓度的AlCl3溶液中滴入2mol/LNaOH溶液时,得到的Al(OH)3沉淀质量与所加NaOH溶液体积(mL)的关系如图所示,
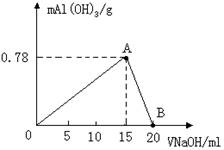
试回答下列问题:
(1)图中A点表示的意义是 ___________
(2)图中B点表示的意义是___________
(3)上述两步总反应用总的离子方程式可表示为:___________
(4)若溶液中有Al(OH)3沉淀0.39g,则此时用去NaOH溶液的体积为___________(写出计算过程)

试回答下列问题:
(1)图中A点表示的意义是 ___________
(2)图中B点表示的意义是___________
(3)上述两步总反应用总的离子方程式可表示为:___________
(4)若溶液中有Al(OH)3沉淀0.39g,则此时用去NaOH溶液的体积为___________(写出计算过程)

略

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 2MgO;②3Mg+N2
2MgO;②3Mg+N2 MgO+H2↑ ⑤Mg3N2 +6H2O ===3Mg(OH)2+2NH3↑
MgO+H2↑ ⑤Mg3N2 +6H2O ===3Mg(OH)2+2NH3↑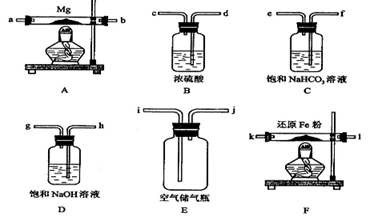
 ;
; 硫酸转移到容量瓶中。
硫酸转移到容量瓶中。 盖上容量瓶塞子,振荡,摇匀。
盖上容量瓶塞子,振荡,摇匀。 ,当产生等质量的气体时,下列说法不正确的是
,当产生等质量的气体时,下列说法不正确的是