题目内容
(1)乙炔是一种重要的化工原料,实验室用电石(CaC2)与水反应来制取乙炔,写出实验室制取乙炔的化学方程式
(2)乙炔分子中碳碳三键比乙烯分子中碳碳双键的键长
CaC2+2H2O-→Ca(OH)2+C2H2↑
CaC2+2H2O-→Ca(OH)2+C2H2↑
,氯乙烯可由乙炔制取,其反应的化学方程式为CH≡CH+HCl
CH2=CHCl
| 催化剂 |
| △ |
CH≡CH+HCl
CH2=CHCl
.| 催化剂 |
| △ |
(2)乙炔分子中碳碳三键比乙烯分子中碳碳双键的键长
短
短
(填长,短),键能大
大
(填大或小).分析:(1)制取装置包括加热和不需加热两种,实验室常用块状固体碳化钙(CaC2)与水反应生成氢氧化钙[Ca(OH)2]和乙炔;乙烯与氯气发生加成反应;
(2)双键键长长于三键,双键键能低于三键.
(2)双键键长长于三键,双键键能低于三键.
解答:解:(1)碳化钙(CaC2)与水反应生成氢氧化钙[Ca(OH)2]和乙炔,配平即可,方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑,乙烯与氯气发生加成反应,生成氯乙烯的反应为:CH≡CH+HCl
CH2=CHCl,故答案为:CaC2+2H2O-→Ca(OH)2+C2H2↑;:CH≡CH+HCl
CH2=CHCl;
(2)双键键长长于三键,双键键能低于三键,故答案为:短;大.
| 催化剂 |
| △ |
| 催化剂 |
| △ |
(2)双键键长长于三键,双键键能低于三键,故答案为:短;大.
点评:本题考查学生乙炔的制备、双键和三键的性质等方面的知识,可以根据所学知识来回答,难度不大.

练习册系列答案
相关题目
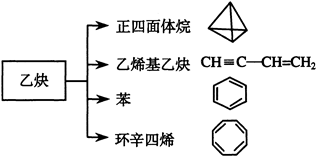
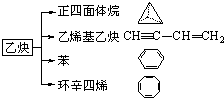 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.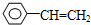
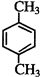

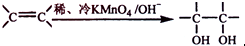 .请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式
.请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式
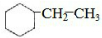
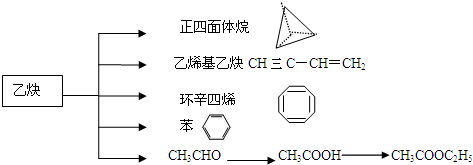
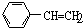 B.
B.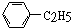 C.
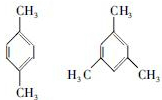
C.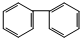 D.
D.
 ,②乙烯基乙炔CH2=CH-C≡CH,③苯
,②乙烯基乙炔CH2=CH-C≡CH,③苯