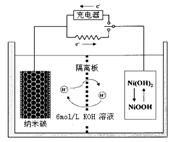
题目内容
已知在室温时,Mg(OH)2的溶度积Ksp=5.6×10-12(mol/L)3,要使0.2mol/l MgSO4溶液中的Mg2+沉淀较为完全[c(Mg2+)<5.6×10-6mol/L],则应向溶液中加入NaOH溶液,使溶液的PH最小为多少?
(2)Mg2+沉淀较为完全是的浓度为5.6×10-6mol/L,已知Ksp=c(Mg2+)×c2(OH-),
则c(OH-)=
=
mol/L═10-3mol/L,
则c(H+)=
=
mol/L=10-11mol/L,
所以pH=-lg(10-11)=11,
答:使溶液的PH最小为11.
则c(OH-)=
|
|
则c(H+)=
| Kw |
| c(OH-) |
| 10-14 |
| 10-3 |
所以pH=-lg(10-11)=11,
答:使溶液的PH最小为11.

练习册系列答案
相关题目
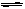 5Ca2+(aq)+3PO43-(aq) +OH-(aq)
5Ca2+(aq)+3PO43-(aq) +OH-(aq)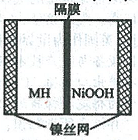
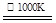 MnFe2O4-X+(X/2)O2
MnFe2O4-X+(X/2)O2