题目内容
25℃时,下列说法正确的是
A.pH =8.3的NaHCO3溶液:c( Na+)>c( HC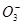 )>c(C
)>c(C 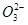 )>c( H2CO3)
)>c( H2CO3)
B.中和同浓度同体积的盐酸和醋酸,消耗的NaOH的物质的量不相同
C.用一定浓度的NaOH溶液滴定氢氟酸,当pH =6时,溶液中c(F—)—c(Na+)=9.9×l0—7 mol/L
D.用NaOH溶液滴定HCI与CH3COOH的混合溶液至中性时,溶液中的酸被完全中和
【答案】
C
【解析】A、pH =8.3的NaHCO3溶液,溶液呈碱性,说明水解大于电离,c( H2CO3)>c(C 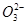 ),A不正确;B、同浓度同体积的盐酸和醋酸中溶质的物质的量相同,中和同浓度同体积的盐酸和醋酸,消耗的NaOH的物质的量相同,B不正确;C、由电荷守恒,c(F—)—c(Na+)=c(H+ )—c(OH―
)=10―6―10―8=9.9×l0—7 mol/L,C正确;D、醋酸是弱酸,中和至中性时,溶液中酸过量,D不正确;选C。
),A不正确;B、同浓度同体积的盐酸和醋酸中溶质的物质的量相同,中和同浓度同体积的盐酸和醋酸,消耗的NaOH的物质的量相同,B不正确;C、由电荷守恒,c(F—)—c(Na+)=c(H+ )—c(OH―
)=10―6―10―8=9.9×l0—7 mol/L,C正确;D、醋酸是弱酸,中和至中性时,溶液中酸过量,D不正确;选C。
考点:电解质溶液

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案
相关题目
 2NH3(g);已知298 K时,
2NH3(g);已知298 K时,

 2NH3(g);已知298 K时,
2NH3(g);已知298 K时,

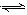 N2O4(g)(正反应为放热反应),若把烧瓶置于100℃的沸水中,下列说法正确的是()。
N2O4(g)(正反应为放热反应),若把烧瓶置于100℃的沸水中,下列说法正确的是()。