题目内容
【题目】铝土矿的主要成分是Al2O3,含有杂质SiO2、Fe2O3、MgO。工业上从铝土矿中提取铝可采用如下工艺流程:
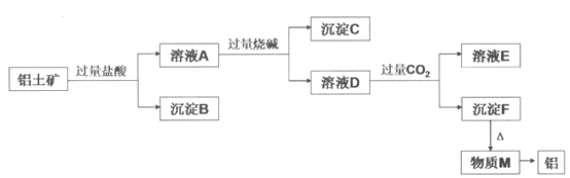
请回答下列问题:
(1)沉淀B的成分是____________(填化学式,下同);
(2)沉淀C的成分是__________;
(3)沉淀F转化为物质M的化学方程式为 _____________________;
(4)溶液D中通入过量CO2生成沉淀F的离子方程式为_____________________________。
【答案】SiO2 Fe(OH)3、Mg(OH)2 2Al(OH)3![]() Al2O3+3H2O AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
Al2O3+3H2O AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
【解析】
铝土矿的主要成分是Al2O3,含有杂质SiO2、Fe2O3、MgO,因Al2O3、SiO2与NaOH溶液反应,MgO、Fe2O3不与NaOH溶液反应;除SiO2不与盐酸反应外,Al2O3、Fe2O3、MgO均与盐酸反应;结合流程可知,加入过量盐酸,溶液A为AlCl3、MgCl2、FeCl3,沉淀B为SiO2,A中加入过量烧碱,沉淀C为Fe(OH)3和Mg(OH)2,溶液D为NaAlO2,D中通入过量二氧化碳,溶液E为NaHCO3,沉淀F为Al(OH)3,加热分解得到M为Al2O3,经电解氧化铝可得到Al,结合题目要求可解答该题。
(1)由上述分析可知,沉淀B的成分是SiO2,故答案为:SiO2;
(2)沉淀C的成分是Fe(OH)3、Mg(OH)2,故答案为:Fe(OH)3、Mg(OH)2;
(3)沉淀F转化为物质M,即由Al(OH)3受热分解为Al2O3的过程,其化学方程式为2Al(OH)3![]() Al2O3+3H2O,故答案为:2Al(OH)3
Al2O3+3H2O,故答案为:2Al(OH)3![]() Al2O3+3H2O;
Al2O3+3H2O;
(4)溶液D中通入过量CO2生成沉淀F的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,故答案为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-。

 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案【题目】(题文)由下列实验及现象不能推出相应结论的是
实验 | 现象 | 结论 | |
A | 加热盛有少量NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸 | 石蕊试纸变蓝 | NH4HCO3固体受热分解,产生的NH3与水反应生成的氨水显碱性 |
B | 向2支盛有1 mL相同浓度AgNO3溶液的试管中分别加入3滴相同浓度的KCl和KI溶液 | 一只试管中产生黄色沉淀,另一支中无明显现象 |
|
C | 向苯酚钠溶液中通入CO2 | 溶液变浑浊 | 相同条件下,碳酸的酸性一定比苯酚强 |
D | 用铂丝蘸取少量某溶液进行焰色反应 | 火焰呈黄色 | 证明该溶液中一定存在Na+和K+ |
A. A B. B C. C D. D

