题目内容
 (2012?长宁区二模)短周期中常见金属X、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用).根据题意完成下列填空:
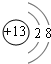
(2012?长宁区二模)短周期中常见金属X、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用).根据题意完成下列填空:(1)X的单质既可与盐酸反应,又可与NaOH溶液反应,X的离子结构示意图为

Al(OH)3=H++AlO2-+H2O
Al(OH)3=H++AlO2-+H2O
.(2)石墨是最常见的碳单质.石墨烯(如图)是单层的石墨,发现它的科学家获得了2010年诺贝尔物理学奖.下列有关石墨烯的叙述正确的是
ag
ag
.a.石墨烯分子中所有原子可以处于同一平面
b.石墨烯中的碳碳键的键角是60°
c.石墨烯中碳原子的化合价为+3
d.石墨烯可导电,说明它是电解质
e.石墨烯的结构与金刚石相似
f. 石墨烯的熔点很低
g.从石墨剥离得石墨烯需克服范德华力
(3)钛是目前金属材料中比强度(强度与密度的比值)最大的金属.其外围电子排布为:3d24s2,可见,钛原子核外有
22
22
种不同运动状态的电子,有7
7
种不同能量的轨道.(4)题干中所示反应的化学方程式为:
4Al+3TiO2+3C
2Al2O3+3TiC
| ||
4Al+3TiO2+3C
2Al2O3+3TiC
.
| ||
分析:(1)能和盐酸和氢氧化钠溶液反应的金属单质是铝,铝是13号元素,其最外层有3个电子,铝原子易失去3个电子生成铝离子;铝的最高价氧化物的水化物是氢氧化铝,氢氧化铝在碱性溶液中以酸的形式电离;
(2)a.根据苯的结构分析;
b.石墨烯中的碳碳键的键角不是60°;
c.石墨烯是单质;
d.单质既不是电解质也不是非电解质;
e.金刚石是空间网状结构;
f.石墨烯是分子晶体,熔点不很低;
g.分子晶体中分子间存在分子间作用力;
(3)原子核外有多少个电子就有多少种运动状态,有多少种能级就有多少种不同能量的轨道;
(4)高温条件下,铝、石墨和二氧化钛反应生成氧化铝和碳化钛.
(2)a.根据苯的结构分析;
b.石墨烯中的碳碳键的键角不是60°;
c.石墨烯是单质;
d.单质既不是电解质也不是非电解质;
e.金刚石是空间网状结构;
f.石墨烯是分子晶体,熔点不很低;
g.分子晶体中分子间存在分子间作用力;
(3)原子核外有多少个电子就有多少种运动状态,有多少种能级就有多少种不同能量的轨道;
(4)高温条件下,铝、石墨和二氧化钛反应生成氧化铝和碳化钛.
解答:解:(1)能和盐酸和氢氧化钠溶液反应的金属单质是铝,铝是13号元素,铝离子原子结构示意图为: ,铝的最高价氧化物的水化物是氢氧化铝,氢氧化铝在碱性溶液中的电离方程式为:Al(OH)3=H++AlO2-+H2O,故答案为:
,铝的最高价氧化物的水化物是氢氧化铝,氢氧化铝在碱性溶液中的电离方程式为:Al(OH)3=H++AlO2-+H2O,故答案为: ,Al(OH)3=H++AlO2-+H2O;
,Al(OH)3=H++AlO2-+H2O;
(2)a.石墨烯的结构和多个苯环相连的结构相似,苯中各原子处于同一平面上,根据苯的结构知,
石墨烯分子中所有原子可以处于同一平面,故正确;
b.石墨烯中的碳碳键的键角是120°,故错误;
c.石墨烯是单质,化合价为0,故错误;
d.石墨烯是单质,所以它既不是电解质也不是非电解质,故错误;
e.石墨烯是平面结构,金刚石是空间网状结构,故错误;
f.石墨烯虽然是分子晶体,但熔点不很低,故错误;
g.石墨属于分子晶体,分子间存在分子间作用力,所以从石墨剥离得石墨烯需克服范德华力,故正确;
故选ag;
(3)原子核外有多少个电子就有多少种运动状态,有多少种能级就有多少种不同能量的轨道,钛是22号元素,其核外有22个电子,所以有22种运动状态,有1s 2s 2p 3s 3p 3d 4s共7种不同能量的轨道,故答案为:22;7;
(4)高温条件下,铝、石墨和二氧化钛反应生成氧化铝和碳化钛,反应方程式为 4Al+3TiO2+3C
2Al2O3+3TiC,故答案为:4Al+3TiO2+3C
2Al2O3+3TiC.
 ,铝的最高价氧化物的水化物是氢氧化铝,氢氧化铝在碱性溶液中的电离方程式为:Al(OH)3=H++AlO2-+H2O,故答案为:
,铝的最高价氧化物的水化物是氢氧化铝,氢氧化铝在碱性溶液中的电离方程式为:Al(OH)3=H++AlO2-+H2O,故答案为: ,Al(OH)3=H++AlO2-+H2O;
,Al(OH)3=H++AlO2-+H2O;(2)a.石墨烯的结构和多个苯环相连的结构相似,苯中各原子处于同一平面上,根据苯的结构知,
石墨烯分子中所有原子可以处于同一平面,故正确;
b.石墨烯中的碳碳键的键角是120°,故错误;
c.石墨烯是单质,化合价为0,故错误;
d.石墨烯是单质,所以它既不是电解质也不是非电解质,故错误;
e.石墨烯是平面结构,金刚石是空间网状结构,故错误;
f.石墨烯虽然是分子晶体,但熔点不很低,故错误;
g.石墨属于分子晶体,分子间存在分子间作用力,所以从石墨剥离得石墨烯需克服范德华力,故正确;
故选ag;
(3)原子核外有多少个电子就有多少种运动状态,有多少种能级就有多少种不同能量的轨道,钛是22号元素,其核外有22个电子,所以有22种运动状态,有1s 2s 2p 3s 3p 3d 4s共7种不同能量的轨道,故答案为:22;7;
(4)高温条件下,铝、石墨和二氧化钛反应生成氧化铝和碳化钛,反应方程式为 4Al+3TiO2+3C
| ||
| ||
点评:本题考查物质结构和性质,难点是判断原子核外电子运动状态的种类、能量的种类,会根据图象分析石墨烯的结构,难度不大.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目