题目内容
(2010?杭州二模)用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U型管的质量差,实验测得m(H):m(O)>1:8.下列对导致这一结果的原因的分析中,一定错误的是( )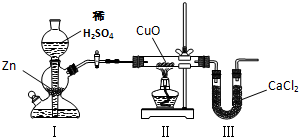

分析:根据所学知识可以知道:在水中氢氧元素的质量比为1:8,而实验中测得氢氧元素的质量比大于1:8,则说明氢元素的质量测多了,或是氧元素的质量测少了;分析图中的装置可以得出:玻璃管减轻的质量就是生成的水中氧元素的质量,U型管增加的质量即为生成的水的质量,水的质量减去氧元素的质量就是氢元素的质量,解答时可以根据这两个方面进行分析.
解答:解:A、锌和稀硫酸反应生成的氢气会带出一部分水蒸气,I、Ⅱ装置之间如果缺少干燥装置会使反应后测得水的质量增加,进而使氢元素的质量增加,而氧元素的质量不变,所以会导致质量比变大,故A正确;
B、III装置后缺少干燥装置,会使空气中的水蒸气进入III装置中,而使测得的水的质量增加,进而使氢元素的质量增加,而对氧元素的质量没有影响,故B正确;
C、我们是通过玻璃管的中固体的质量减少来确定氧元素的质量,所以Ⅱ装置中玻璃管内有水冷凝,那么由于有水的存在而使测得玻璃管质量变化小,从而导致测得的氧元素质量减小,故C正确;
D、CuO没有全部被还原,只会使反应后生成的水的质量也随之减少,而对于氢氧元素的质量没有影响,所以对实验结果没有影响,故D错误.
故选D.
B、III装置后缺少干燥装置,会使空气中的水蒸气进入III装置中,而使测得的水的质量增加,进而使氢元素的质量增加,而对氧元素的质量没有影响,故B正确;
C、我们是通过玻璃管的中固体的质量减少来确定氧元素的质量,所以Ⅱ装置中玻璃管内有水冷凝,那么由于有水的存在而使测得玻璃管质量变化小,从而导致测得的氧元素质量减小,故C正确;
D、CuO没有全部被还原,只会使反应后生成的水的质量也随之减少,而对于氢氧元素的质量没有影响,所以对实验结果没有影响,故D错误.
故选D.
点评:熟练掌握氢气还原氧化铜的性质和实验,能够根据实验装置图分析出各装置的作用,然后作出正确的判断,这是我们必须具备的能力.

练习册系列答案
相关题目
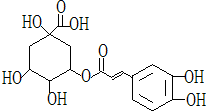 (2010?杭州二模)金银花是治疗和预防甲型H1N1的常见中草药,有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构式见图,下列有关绿原酸的说法不正确的是( )
(2010?杭州二模)金银花是治疗和预防甲型H1N1的常见中草药,有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构式见图,下列有关绿原酸的说法不正确的是( )
 (2010?杭州二模)“化学与生活”模块
(2010?杭州二模)“化学与生活”模块