题目内容
已知高锰酸钾、二氧化锰在酸性条件下能将草酸钠(Na2C2O4)氧化:
MnO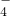 +C2O
+C2O +H+→Mn2++CO2↑+H2O(未配平);
+H+→Mn2++CO2↑+H2O(未配平);
MnO2+C2O +H+→Mn2++CO2↑+H2O(未配平).
+H+→Mn2++CO2↑+H2O(未配平).
为测定某软锰矿中二氧化锰的质量分数,准确称量1.20g软锰矿样品,加入2.68g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应后冷却,将所得溶液转移到容量瓶中用蒸馏水稀释至刻度,从中取出25.0mL,用0.0200mol?L-1高锰酸钾溶液进行滴定.当加入20.0mL溶液时恰好完全反应,试根据以上信息完成下列各题:
(1)配平上述两个离子方程式:
______MnO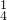 +______C2O
+______C2O +______H+═______Mn2++______CO2↑+______H2O;
+______H+═______Mn2++______CO2↑+______H2O;
______MnO2+______C2O +______H+═______Mn2++______CO2↑+______H2O.
+______H+═______Mn2++______CO2↑+______H2O.
(2)欲求得软锰矿中二氧化锰的质量分数,还缺一个数据,这个数据是______(填数据所代表的意义).
(3)若该数据的数值为250,求该软锰矿中二氧化锰的质量分数(写出计算过程).
解:(1)反应中MnO4-→Mn2+,锰元素化合价由+7价降低为+2价,共降低5价,C2O42-→CO2,碳元素化合价由+3价升高为+4,共升高2价,化合价最小公倍数为10,故MnO4-系数为2,C2O42-系数为5,再根据元素守恒可知Mn2+系数为2、CO2系数为10,根据电荷守恒可知H+系数为16,根据氢元素守恒可知H2O系数为8,配平后离子方程式为2MnO4-+5C2O42-+16H+=2Mn2++10CO2+8H2O.
反应中MnO2→Mn2+,锰元素化合价由+4价降低为+2价,共降低2价,C2O42-→CO2,碳元素化合价由+3价升高为+4,共升高2价,化合价最小公倍数为2,故MnO2系数为1,C2O42-系数为1,再根据元素守恒可知Mn2+系数为1、CO2系数为2,根据电荷守恒可知H+系数为4,根据氢元素守恒可知H2O系数为2,配平后离子方程式为MnO2+C2O42-+4H+=Mn2++2CO2+2H2O.
故答案为:2、5、16=2、10、8; 1、1、4=1、2、2.
(2)锰酸钾溶液滴定稀释后25.0mL溶液中未反应的C2O42-,需要知道总共剩余的C2O42-,才能计算二氧化锰的质量分数,还需要知道稀释后溶液的体积,即该体积为容量瓶的容积.
故答案为:容量瓶的容积.
(3)n(C2O42-)=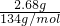 =0.02 mol,
=0.02 mol,
滴定250 mL稀释后的溶液,消耗n(MnO4-)=0.0200 mol?L-1×0.02 L×10=0.004 mol,
根据氧化还原反应中得失电子数相等,有:
n(MnO2)×2+0.004 mol×5=0.02 mol×2,
所以n(MnO2)=0.01 mol,
所以w(MnO2)=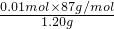 ×100%=72.5%.
×100%=72.5%.
答:该软锰矿中二氧化锰的质量分数为72.5%.
分析:(1)反应中MnO4-→Mn2+,锰元素化合价由+7价降低为+2价,共降低5价,C2O42-→CO2,碳元素化合价由+3价升高为+4,共升高2价,化合价最小公倍数为10,故MnO4-系数为2,C2O42-系数为5,再根据元素守恒、电荷守恒确定其它物质的系数.
反应中MnO2→Mn2+,锰元素化合价由+4价降低为+2价,共降低2价,C2O42-→CO2,碳元素化合价由+3价升高为+4,共升高2价,化合价最小公倍数为2,故MnO2系数为1,C2O42-系数为1,再根据元素守恒、电荷守恒确定其它物质的系数.
(2)锰酸钾溶液滴定稀释后25.0mL溶液中未反应的C2O42-,需要知道总共剩余的C2O42-,才能计算二氧化锰的质量分数,还需要知道稀释后溶液的体积.
(3)计算出滴定250 mL稀释后的溶液,消耗的n(MnO4-),MnO2与MnO4-获得的电子等于2.68g草酸钠提供的电子,即n(MnO2)×2+n(MnO4-)×5=n(C2O42-)×2,据此计算n(MnO2),进而计算MnO2质量分数.
点评:考查氧化还原反应配平、氧化还原反应滴定运用、化学计算等,难度中等,(3)中利用电子转移守恒计算,比利用关系式计算更简便,注意氧化还原反应计算中守恒思想的运用.
反应中MnO2→Mn2+,锰元素化合价由+4价降低为+2价,共降低2价,C2O42-→CO2,碳元素化合价由+3价升高为+4,共升高2价,化合价最小公倍数为2,故MnO2系数为1,C2O42-系数为1,再根据元素守恒可知Mn2+系数为1、CO2系数为2,根据电荷守恒可知H+系数为4,根据氢元素守恒可知H2O系数为2,配平后离子方程式为MnO2+C2O42-+4H+=Mn2++2CO2+2H2O.
故答案为:2、5、16=2、10、8; 1、1、4=1、2、2.
(2)锰酸钾溶液滴定稀释后25.0mL溶液中未反应的C2O42-,需要知道总共剩余的C2O42-,才能计算二氧化锰的质量分数,还需要知道稀释后溶液的体积,即该体积为容量瓶的容积.
故答案为:容量瓶的容积.
(3)n(C2O42-)=
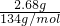 =0.02 mol,
=0.02 mol,滴定250 mL稀释后的溶液,消耗n(MnO4-)=0.0200 mol?L-1×0.02 L×10=0.004 mol,
根据氧化还原反应中得失电子数相等,有:
n(MnO2)×2+0.004 mol×5=0.02 mol×2,
所以n(MnO2)=0.01 mol,
所以w(MnO2)=
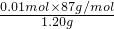 ×100%=72.5%.
×100%=72.5%.答:该软锰矿中二氧化锰的质量分数为72.5%.
分析:(1)反应中MnO4-→Mn2+,锰元素化合价由+7价降低为+2价,共降低5价,C2O42-→CO2,碳元素化合价由+3价升高为+4,共升高2价,化合价最小公倍数为10,故MnO4-系数为2,C2O42-系数为5,再根据元素守恒、电荷守恒确定其它物质的系数.
反应中MnO2→Mn2+,锰元素化合价由+4价降低为+2价,共降低2价,C2O42-→CO2,碳元素化合价由+3价升高为+4,共升高2价,化合价最小公倍数为2,故MnO2系数为1,C2O42-系数为1,再根据元素守恒、电荷守恒确定其它物质的系数.
(2)锰酸钾溶液滴定稀释后25.0mL溶液中未反应的C2O42-,需要知道总共剩余的C2O42-,才能计算二氧化锰的质量分数,还需要知道稀释后溶液的体积.
(3)计算出滴定250 mL稀释后的溶液,消耗的n(MnO4-),MnO2与MnO4-获得的电子等于2.68g草酸钠提供的电子,即n(MnO2)×2+n(MnO4-)×5=n(C2O42-)×2,据此计算n(MnO2),进而计算MnO2质量分数.
点评:考查氧化还原反应配平、氧化还原反应滴定运用、化学计算等,难度中等,(3)中利用电子转移守恒计算,比利用关系式计算更简便,注意氧化还原反应计算中守恒思想的运用.

练习册系列答案
相关题目
 品,加入2.68 g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应后冷却,将所得溶液转移到容量瓶中用蒸馏水稀释至刻度,从中取出25.0 mL,用0.0200 mol·L-1高锰酸钾溶液进行滴定。当加入20.0 mL溶液时恰好完全反应,试根据以上信息完成下列各题:
品,加入2.68 g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应后冷却,将所得溶液转移到容量瓶中用蒸馏水稀释至刻度,从中取出25.0 mL,用0.0200 mol·L-1高锰酸钾溶液进行滴定。当加入20.0 mL溶液时恰好完全反应,试根据以上信息完成下列各题: 2++___CO2↑+__H2O。
2++___CO2↑+__H2O。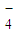 +C2O
+C2O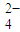 +H+→Mn2++CO2↑+H2O(未配平);
+H+→Mn2++CO2↑+H2O(未配平);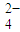 +H+→Mn2++CO2↑+H2O(未配平).
+H+→Mn2++CO2↑+H2O(未配平).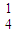 +______C2O
+______C2O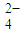 +______H+═______Mn2++______CO2↑+______H2O;
+______H+═______Mn2++______CO2↑+______H2O;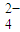 +______H+═______Mn2++______CO2↑+______H2O.
+______H+═______Mn2++______CO2↑+______H2O.