题目内容
向50mL18mol·L-1的硫酸中加入足量的铜片并加热,被还原的硫酸的物质的量是
- A.等于0.9mol
- B.大于0.45mol,小于0.9mol
- C.等于0.45mol
- D.小于0.45mol
D
铜和浓硫酸反应的方程式为Cu+2H2SO4(浓)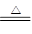 CuSO4+2H2O+SO2↑,由于随着反应进行,浓硫酸的浓度会逐渐降低,而稀硫酸是不能氧化铜的。浓硫酸的物质的量是0.05L×18mol/L=0.9mol,根据反应式可知理论上被还原的硫酸是0.45mol,所以实际上被还原的硫酸应小于0.45mol。答案选D。
CuSO4+2H2O+SO2↑,由于随着反应进行,浓硫酸的浓度会逐渐降低,而稀硫酸是不能氧化铜的。浓硫酸的物质的量是0.05L×18mol/L=0.9mol,根据反应式可知理论上被还原的硫酸是0.45mol,所以实际上被还原的硫酸应小于0.45mol。答案选D。
铜和浓硫酸反应的方程式为Cu+2H2SO4(浓)
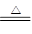 CuSO4+2H2O+SO2↑,由于随着反应进行,浓硫酸的浓度会逐渐降低,而稀硫酸是不能氧化铜的。浓硫酸的物质的量是0.05L×18mol/L=0.9mol,根据反应式可知理论上被还原的硫酸是0.45mol,所以实际上被还原的硫酸应小于0.45mol。答案选D。
CuSO4+2H2O+SO2↑,由于随着反应进行,浓硫酸的浓度会逐渐降低,而稀硫酸是不能氧化铜的。浓硫酸的物质的量是0.05L×18mol/L=0.9mol,根据反应式可知理论上被还原的硫酸是0.45mol,所以实际上被还原的硫酸应小于0.45mol。答案选D。 
练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案
相关题目
对下列事实的解释正确的是( )
| A、氯气可以使湿润的有色布条褪色,是因为氯气具有漂白性 | B、用氢氟酸雕刻玻璃,是由于氢氟酸能与二氧化硅反应 | C、向50mL18mol?L-1 的H2SO4溶液中加入足量的铜片加热充分反应后,被还原的H2SO4的物质的量等于0.45mol | D、常温下,浓硝酸可以用铝制容器贮存,说明铝与浓硝酸不反应 |
对下列事实的解释错误的是( )
| A、在蔗糖中加入浓H2SO4后出现发黑现象,说明浓硫酸具有脱水性 | B、向50mL18mol?L-1的H2SO4溶液中加入足量的铜片加热充分反应后,被还原的H2SO4的物质的量小于0.45mol | C、常温下,浓H2SO4可以用铝制容器贮存,说明铝与浓H2SO4不反应 | D、反应CuSO4+H2S═CuS+H2SO4能进行,说明CuS既不溶于水也不溶于稀H2SO4 |
对下列事实的解释不正确的是( )
| A、在蔗糖中加入浓H2SO4后出现发黑现象,说明浓硫酸具有脱水性 | B、常温下,浓H2SO4可以用铝制容器贮存,说明铝与浓H2SO4不反应 | C、向50mL18mol?L-1 的H2SO4溶液中加入足量的铜片加热充分反应后,被还原的H2SO4的物质的量小于0.45mol | D、实验室用MnO2和浓盐酸反应制取Cl2中含有少量的HCl气体杂质,可通过饱和的食盐水除去 |