题目内容
在0.10mol·L-1NH3·H2O溶液中,加入少量NH4Cl晶体后,引起的变化是
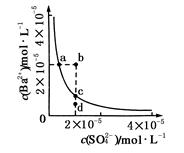

| A.NH3·H2O的电离程度减小 | B.NH3·H2O的电离常数增大 |
| C.溶液的导电能力不变 | D.溶液的pH增大 |
D
试题分析:溶液中发生的水解电离反应为NH3·H2O+H2O
 NH4++OH- ;A、加入NH4Cl后NH4+浓度增大反应逆向进行,故NH3·H2O电离程度减少,故A错误;B、溶液的电离常数只与温度有关,不随溶液浓度变化,故B错误。C、溶液的导电能力与溶液中的离子浓度有关,加入NH4Cl晶体后NH4+浓度增大导电能力增大,故C错误;D、加入NH4Cl晶体后反应逆向进行OH-浓度降低,溶液pH减小,故D正确。
NH4++OH- ;A、加入NH4Cl后NH4+浓度增大反应逆向进行,故NH3·H2O电离程度减少,故A错误;B、溶液的电离常数只与温度有关,不随溶液浓度变化,故B错误。C、溶液的导电能力与溶液中的离子浓度有关,加入NH4Cl晶体后NH4+浓度增大导电能力增大,故C错误;D、加入NH4Cl晶体后反应逆向进行OH-浓度降低,溶液pH减小,故D正确。
练习册系列答案
 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案
相关题目



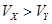
 CH3COO-+H+ ΔH>0
CH3COO-+H+ ΔH>0