题目内容
已知A、B均为可溶性正盐,A的水溶液为浅绿色,B为硫化物,在一定条件下A、B的溶液间可以发生如图所示的变化:
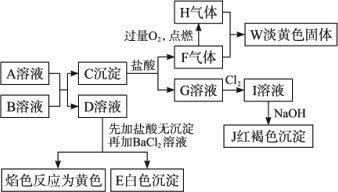
(1)写出下列物质的化学式:A________,D________.
(2)检验D溶液中所含的阴离子,能否滴加盐酸酸化的BaCl2溶液?请简述理由.
(3)写出下列变化的化学方程式(是离子反应的,写出离子方程式):
①F+H![]() W:________;
W:________;
②C沉淀+盐酸:________;
③G溶液与NaOH溶液反应开始得到的沉淀J:________.
解析:
|
答案:(1)FeSO4 Na2SO4 (2)不能,不加入足量的盐酸,不能排除 解析:从总体上观察,可以寻求突破口为:J为红褐色沉淀,应该是Fe(OH)3,回推知G溶液含Fe2+,F为H2S(结合F与过量氧气反应生成H气体,氧气不足时生成淡黄色沉淀W,则W为单质硫,据此判断气体F为H2S),这是本题的突破口,依据此展开讨论. |

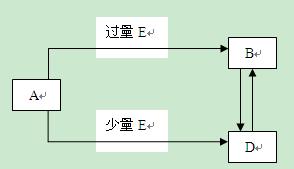
X、Y、Z、W均为含有10电子的微粒,W为金属阳离子,X、Y、Z常温下为气体,
(1)已知: W + X + H2O → 白色沉淀。
①若实验室用下图所示装置、干燥和收集装置制取并收集干燥的X,A中分液漏斗中的液态试剂的仪器的名称是________,仪器的连接顺序为a→________________________;
②由W离子形成的可溶性盐WCln,其水溶液显_________性,原因是(用离子方程式表示)_____________________________________________________
③为进一步确定W,进行如下实验,请补全实验操作、现象和结论:取上述白色沉淀少量置于试管中,_____________________________________________________
(2)常温下,取10 mLpH= a的Y的稀溶液,加水稀释时pH随溶液体积V的变化如图所示,则①Y的化学式为__________。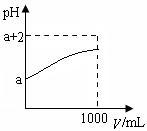
②下列有关Y的叙述正确的是__________
| A.Y溶于水后部分发生电离 |
| B.Y的水溶液中滴加石蕊试液会变红 |
| C.稀释后溶液中所有离子的浓度均减小 |
| D.稀释后,阴离子的物质的量浓度之和不变 |
(用实际离子符号表示)
(3)已知H2的燃烧热为285.8 kJ·mol-1。现有Z和H2的混合气体共0.2 mol,与O2完全燃烧生成H2O(l)和CO2(g),转移电子的物质的量为1.0 mol,放出的热量为117.6 kJ。写出Z完全燃烧的热化学反应方程式__________________________________
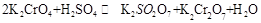
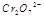 在水溶液中为红色,
在水溶液中为红色,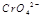 在水溶液中为黄色。某条件下该反应建立平衡后,体系为两种离子的混合液,颜色为橙色。
在水溶液中为黄色。某条件下该反应建立平衡后,体系为两种离子的混合液,颜色为橙色。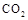 ,能有效地利用资源,并减少空气中的温室气体。工业上正在研究利用
,能有效地利用资源,并减少空气中的温室气体。工业上正在研究利用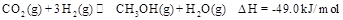
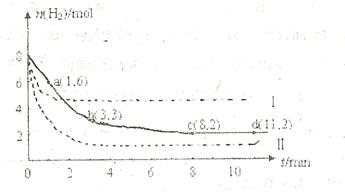
 充入一容积为2L的密闭容器中,测得H
充入一容积为2L的密闭容器中,测得H