题目内容
【题目】一定条件下,在水溶液中1molCl-,ClOx(x=1,2,3,4)的能量(kJ)相对大小如图所示.下列有关说法正确的是( )
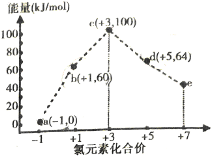
A.e是ClO3-
B.b→a+c反应的活化能为60kJmol-1
C.a,b,c,d,e中c最稳定
D.b→a+d反应的热化学方程式为3ClO-(aq)=ClO3-(aq)+2Cl-(aq)△H=-116kJmol-1
【答案】D
【解析】
试题分析:A、D中Cl元素化合价为+7价,而ClO3-中Cl元素化合价为+5价,故A错误;B、b→a+c反应的活化能为40kJmol-1,故B错误;C、a,b,c,d,e中a能量最低,所以最稳定,故C错误;D、b→a+d,根据转移电子守恒得该反应方程式为3ClO-=ClO3-+2Cl-,反应热 = (64 kJ/mol + 2 × 30 kJ/mol) - 3 × 60 kJ/mol = -116kJ/mol,所以该热化学反应方程式为3ClO-(aq) = ClO3-(aq) + 2Cl-(aq) △H = -116 kJ/mol,故D正确;故选D。

练习册系列答案
相关题目
