题目内容
工业盐中含有NaNO2,外观和食盐相似,有咸味,人若误食会引起中毒,致死量为0.3~0.5g.已知NaNO2能发生如下反应(方程式已配平):2NO2-+xI-+yH+=2NO↑+I2+zH2O,请回答下列问题:
(1)上述反应中,x的数值是
(2)根据上述反应,可用化学试纸及生活中常见物质进行实验来鉴别工业盐和食盐,现有碘化钾淀粉试纸,则还需选用的生活中常见物质的名称为
(3)某工厂废切削液中含有2%~5%的NaNO2,直接排放会造成水污染,但加入下列物质中的某一种就能使NaNO2转化为不引起污染的N2,该物质是
A.NaCl B.KMnO4 C.NH4Cl D.浓硫酸
所发生反应的离子方程式为
(1)上述反应中,x的数值是
2
2
,根据是碘元素质量守恒;
碘元素质量守恒;
;y的数值是4
4
,根据是电荷守恒
电荷守恒
.(2)根据上述反应,可用化学试纸及生活中常见物质进行实验来鉴别工业盐和食盐,现有碘化钾淀粉试纸,则还需选用的生活中常见物质的名称为
食醋
食醋
.(3)某工厂废切削液中含有2%~5%的NaNO2,直接排放会造成水污染,但加入下列物质中的某一种就能使NaNO2转化为不引起污染的N2,该物质是
C
C
.A.NaCl B.KMnO4 C.NH4Cl D.浓硫酸
所发生反应的离子方程式为
NH4++NO2 -=N2+2H2O
NH4++NO2 -=N2+2H2O
.分析:(1)根据或碘元素质量守恒以及电荷守恒;
(2)根据题目信息,需要H+;
(3)根据氧化还原反应原理;
(2)根据题目信息,需要H+;
(3)根据氧化还原反应原理;
解答:解:(1)因化学方程式式碘元素质量守恒以及电荷守恒,故答案为:2;碘元素质量守恒; 4;电荷守恒;
(2)因题目信息提示,该反应2NO2-+xI-+yH+=2NO↑+I2+zH2O在酸性条件下发生,故答案为:食醋;
(3)因NaNO2转化为不引起污染的N2的过程中N的化合价降低,另一物质化合价必升高,
故答案为:C;NH4++NO2 -=N2+2H2O.
(2)因题目信息提示,该反应2NO2-+xI-+yH+=2NO↑+I2+zH2O在酸性条件下发生,故答案为:食醋;
(3)因NaNO2转化为不引起污染的N2的过程中N的化合价降低,另一物质化合价必升高,
故答案为:C;NH4++NO2 -=N2+2H2O.
点评:本题主要考查了氧化还原反应的知识,考查的方式比较灵活,能较好的体现学生运用知识的能力.

练习册系列答案
相关题目
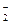 +xI—+yH+=bNO↑+cI2+zH2O,
+xI—+yH+=bNO↑+cI2+zH2O,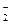 +xI-+yH+=bNO↑+cI2+zH2O,请回答下列问题:
+xI-+yH+=bNO↑+cI2+zH2O,请回答下列问题: 的数值分别是 (全对才给分)。
的数值分别是 (全对才给分)。 。
。 +xI-+yH+=bNO↑+cI2+zH2O,
+xI-+yH+=bNO↑+cI2+zH2O,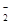 + xI- + yH+
= 2NO↑+ I2 +
zH2O,请回答下列问题:
+ xI- + yH+
= 2NO↑+ I2 +
zH2O,请回答下列问题: