题目内容
【题目】(1)NaBH4(s)与H2O(l)反应生成NaBO2(s)和H2(g),在25 ℃、101 kPa下,已知每消耗3.8 g NaBH4(s)放热21.6 kJ,该反应的热化学方程式是______________________。
(2)降低温度,将NO2(g)转化为N2O4(l),再制备浓硝酸。
①已知:2NO2(g)![]() N2O4(g) ΔH1 2NO2(g)
N2O4(g) ΔH1 2NO2(g)![]() N2O4(l) ΔH2
N2O4(l) ΔH2
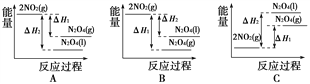
下列能量变化示意图中,正确的是(选填字母)________。
②N2O4与O2、H2O化合的化学方程式是___________________________________。
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是_______________________。
【答案】 NaBH4(s)+2H2O(l)===NaBO2(s)+4H2(g) ΔH=-216 kJ/mol A 2N2O4+O2+2H2O===4HNO3 4CuCl(s)+O2(g)===2CuCl2(s)+2CuO(s) ΔH=-177.6 kJ·mol-1
【解析】试题分析:(1)每消耗3.8 g NaBH4(s)放热21.6 kJ,则消耗1mol NaBH4(s)放热216 kJ;(2) ①降低温度,将NO2(g)转化为N2O4(l),说明2NO2(g)![]() N2O4(g)反应放热;2NO2(g)
N2O4(g)反应放热;2NO2(g)![]() N2O4(l),气体变为液体放热。②N2O4与O2、H2O化合生成硝酸。(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体,根据元素守恒,黑色固体是氧化铜。
N2O4(l),气体变为液体放热。②N2O4与O2、H2O化合生成硝酸。(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体,根据元素守恒,黑色固体是氧化铜。
解析:(1)每消耗3.8 g NaBH4(s)放热21.6 kJ,则消耗1mol NaBH4(s)放热216 kJ,该反应的热化学方程式是NaBH4(s)+2H2O(l)===NaBO2(s)+4H2(g) ΔH=-216 kJ/mol;
(2) ①降低温度,将NO2(g)转化为N2O4(l),说明2NO2(g)![]() N2O4(g)反应放热;2NO2(g)
N2O4(g)反应放热;2NO2(g)![]() N2O4(l),气体变为液体放热,故A正确。
N2O4(l),气体变为液体放热,故A正确。
②N2O4与O2、H2O化合生成硝酸,反应方程式为2N2O4+O2+2H2O===4HNO3。(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体,根据元素守恒,黑色固体是氧化铜。
反应方程式为4CuCl+O2===2CuCl2+2CuO,每消耗1 mol CuCl(s),放热44.4 kJ,消耗4 mol CuCl(s),放热177.6 kJ,反应热化学方程式是4CuCl(s)+O2(g)===2CuCl2(s)+2CuO(s) ΔH=-177.6 kJ·mol-1。

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案


