题目内容
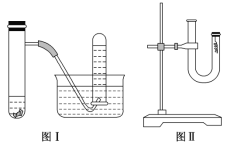
【题目】甲同学采用如图Ⅰ所示装置验证铜与稀硝酸的反应,并用排水法收集NO气体。
(1)反应过程中的实验现象是__________________________________________________。
(2)乙同学认为虽然收集到的气体为一氧化氮,但并不能说明反应中一定生成一氧化氮。你认为他的理由是______________________________________________________________。
(3)丙同学采用如图Ⅱ所示装置进行实验,证明了铜与稀硝酸反应生成一氧化氮。该同学的步骤如下表所示,请回答实验中的有关问题。
实验步骤 | 问题 |
①从U形管左端加入稀硝酸,直至充满U形管右端 | ______ |
②用附有铜丝的胶塞塞住U形管右端,观察现象 | 实验现象是______________ |
③待反应停止后打开胶塞,观察实验现象 | 打开胶塞后的实验现象是_______________________ |
(4)从环境保护的角度看,丙同学的实验存在__________缺陷?你认为应如何改进__________?
【答案】铜片逐渐溶解,溶液由无色变为蓝色,具支试管内液面上空出现少量红棕色气体,水槽试管内液面下降,收集到无色气体 若反应产生NO2,3NO2+H2O=2HNO3+NO,排水收集到的NO为NO2与H2O反应所得 U形管右端收集到无色气体,液面下降 铜丝溶解,溶液变蓝色 U形管左端液面上升 无色气体遇到空气变为红棕色气体 丙同学实验中没有尾气吸收装置;应在胶塞上安装一带活塞的导管并接入盛有O2的集气瓶中(合理均可)。
【解析】
(1)根据铜与稀硝酸的反应判断实验现象;
(2)根据观察到的现象确定并写出反应方程式;
(3)根据生成物的颜色推断现象;根据一氧化氮的性质推断现象;
(4)丙同学实验存在一定的缺陷,生成的NO进入空气中污染大气,同时生成的红棕色NO2被空气稀释颜色较浅,效果不明显,结合原理进行改进。
(1)铜和稀硝酸反应的方程式为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,则反应过程中的实验现象是铜片逐渐溶解,溶液由无色变为蓝色,具支试管内液面上空出现少量红棕色气体,水槽试管内液面下降,收集到无色气体;
(2) 若反应产生的是NO2,与水反应也能产生NO,3NO2+H2O=2HNO3+NO,排水收集到的NO为NO2与H2O反应所得;
(3)①从U形管左端加入稀硝酸,直至充满U形管右端,U形管右端收集到无色气体,液面下降;
②用附有铜丝的胶塞塞住U形管右端,观察现象:铜丝溶解,溶液变蓝色;
③待反应停止后打开胶塞,观察实验现象:U形管左端液面上升;
(4)从环境保护的角度看,丙同学的实验存在的缺陷为:无色气体遇到空气变为红棕色气体;改进方案为丙同学实验中没有尾气吸收装置;应在胶塞上安装一带活塞的导管并接入盛有O2的集气瓶中。