题目内容
硫化氢的水溶液中有如下动态平衡:H2S![]() H++HS-;HS-
H++HS-;HS-![]() H++S2- H2O
H++S2- H2O![]() H++OH-
H++OH-
在物质的量浓度为0.1 mol·L-1的H2S溶液中,下列各离子间的关系正确的是( )
A.c(H+)=c(HS-)+
C.c(H+)=c(HS-)+
解析:H2S溶于水生成的氢硫酸为二元酸,所以分步电离。电离出的阴、阳离子所带的正、负电荷相等。又因为第一步电离生成的HS-要继续进行第二步电离,第一步电离出的c(HS-)相当于最后溶液中c(HS-)与c(S2-)之和,所以c(H+)=c(HS-)+
答案:A

练习册系列答案
相关题目
|
硫化氢的水溶液中有如下动态平衡: H2S 在物质的量浓度为0.1 mol·L-1的H2S溶液中,下列各离子间的关系正确的是 | |
| [ ] | |
A. |
c (H+)=c(HS-)+2c(S2-)+c(OH-) |
B. |
2c(H+)=2c(HS-)+c(S2-)+2c(OH-) |
C. |
c (H+)=c(HS-)+2c(S2-) |
D. |
c (H+)=2c(S2-)+c(OH-) |
 H++HS-;HS-
H++HS-;HS-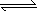 H++S2-;H2O
H++S2-;H2O H++OH-
H++OH-