题目内容
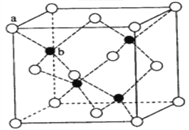
【题目】现有A、B、C三种烃,其球棍模型如下图:

(l)等质量的以上三种物质完全燃烧时,消耗O2的量最多的是______(填分子式),该烃与氧气反应的化学方程式为_________;
(2)等质量的以上三种物质燃烧时,生成二氧化碳最多的是_____(填结构简式), 生成水最多的是_______(填结构式);
(3)相同状况下,等体积的以上下种物质完全燃烧时,消耗O2的量最多的是_____(填物质名称),该烃电子式为__________。
【答案】 CH4 CH4+2O2![]() CO2+2H2O CH2=CH2
CO2+2H2O CH2=CH2 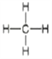 乙烷
乙烷 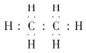
【解析】据球棍模型可知A为CH4,B为C2H4,C为C2H6。则
(1)等质量的烃CxHy完全燃烧时,氢元素的质量分数越大,耗氧量越大。CH4、C2H4、C2H6中的y/x依次为4/1、4/2、6/2,故CH4耗O2最多,方程式为CH4+2O2![]() CO2+2H2O;(2)等质量的以上三种物质燃烧时,物质含有的碳元素的含量越大,其中碳元素的质量越多,其燃烧产生的CO2就越多,由于乙烯中H元素的含量最小,所以其C元素的含量最高,所以等质量时其燃烧产生的CO2最多,结构简式为CH2=CH2;等质量的烃CxHy完全燃烧时,氢元素的质量分数越大,生成的水越多,根据以上分析可知应该是甲烷,结构式为
CO2+2H2O;(2)等质量的以上三种物质燃烧时,物质含有的碳元素的含量越大,其中碳元素的质量越多,其燃烧产生的CO2就越多,由于乙烯中H元素的含量最小,所以其C元素的含量最高,所以等质量时其燃烧产生的CO2最多,结构简式为CH2=CH2;等质量的烃CxHy完全燃烧时,氢元素的质量分数越大,生成的水越多,根据以上分析可知应该是甲烷,结构式为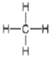 ;(3)等体积的烃CxHy完全燃烧时,(x+y/4)的值越大,耗氧量越大,CH4、C2H4、C2H6的(x+y/4)依次为1+4/4=2、2+4/4=3、2+6/4=3.5,故C2H6耗O2最多,乙烷的电子式为
;(3)等体积的烃CxHy完全燃烧时,(x+y/4)的值越大,耗氧量越大,CH4、C2H4、C2H6的(x+y/4)依次为1+4/4=2、2+4/4=3、2+6/4=3.5,故C2H6耗O2最多,乙烷的电子式为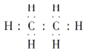 。
。

 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案【题目】苯甲醛在医药、染料、香料等行业有着广泛的应用。实验室通过下图所示的流程由甲苯氧化制备苯甲醛。
试回答下列问题:
(1)Mn2O3氧化甲苯的反应需要不断搅拌,搅拌的作用是______________。
(2)甲苯经氧化后得到的混合物通过结晶、过滤进行分离。该过程中需将混合物冷却,其目的是__________________________。
(3)实验过程中,可循环使用的物质分别为_______、_______。
(4)实验中分离甲苯和苯甲醛采用的操作Ⅰ是______________,其原理是______________。
(5)实验中发现,反应时间不同苯甲醛的产率也不同(数据见下表)。
反应时间/h | 1 | 2 | 3 | 4 | 5 |
苯甲醛产率/% | 76.0 | 87.5 | 83.6 | 72.5 | 64.8 |
请结合苯甲醛的结构,分析当反应时间过长时,苯甲醛产率下降的原因____________