题目内容
在一密闭容器中加入A和B,各物质的物质的量浓度随着反应的进行,如图所示。下列说法不正确的是
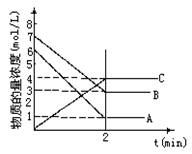
 A.该反应的化学方程式为5A+4B 4C
A.该反应的化学方程式为5A+4B 4C
B.2min时,该反应达到平衡,此时A、B、C的浓度比为5:4:4
C.用B的浓度变化表示0-2min时间内的速率为2mol/(L·min)
D.2min前,正反应速率逐渐减小,逆反应速率逐渐增大,但是正反应速率大于逆反应速率。
【答案】
B
【解析】根据图像可知,反应进行到2min是,物质的浓度不在发生变化,说明反应达到平衡状态。其中AB的浓度减小,C的浓度最大,其浓度的变化量分别是6mol/L-1mol/L=5mol/L、7mol/L-3mol/L=4mol/L、4mol/L-0=4mol/L,所以反应式为5A+4B 4C,A正确,B不正确。B的反应速率是4mol/L÷2min=2mol/(L·min),C正确。由于反应是向正反应方向移动的,所以D也是正确的,答案选B。
4C,A正确,B不正确。B的反应速率是4mol/L÷2min=2mol/(L·min),C正确。由于反应是向正反应方向移动的,所以D也是正确的,答案选B。

练习册系列答案
相关题目
在一密闭容器中加入A、B、C三种气体,保持一定温度,在t1~t4时刻测得各物质的浓度如下表.据此判断下列结论正确的是( )
|
(2008?肇庆一模)在一密闭容器中加入A、B、C三种气体,保持一定温度,在t1~t4(s)时刻测得各物质的浓度如下表.据此下列结论正确的是( )
|
在一密闭容器中加入A、B、C三种气体,在温度为T K和(T+10)K时,测得各物质的浓度如表.据此下列结论正确的是( )
| ||||||||||||||||||||||||||||||
在一密闭容器中加入A、B、C三种气体,保持一定温度,在t1~t4时刻测得各物质的浓度如下表。据此判断下列结论正确的是( )
|
测定时刻/s |
t1 |
t2 |
t3 |
t4 |
|
c(A)/(mol·L-1) |
6 |
3 |
2 |
2 |
|
c(B)/(mol·L-1) |
5 |
3.5 |
3 |
3 |
|
c(C)/(mol·L-1) |
1 |
2.5 |
3 |
3 |
A.在t3 时刻反应已经停止
B.A的转化率比B的转化率低
C.在容器中发生的反应为2A+B? ?2C
?2C
D.在t2~t3内A的平均反应速率为1mol·L-1·s-1

