题目内容
下列说法不正确的是
A.硫酸可用于精炼石油、金属加工之前的酸洗
B.氨易液化,常用作制冷剂
C.二氧化硫可用来加工食品,以使食品增白
D.硅是半导体材料,用作光电池
练习册系列答案
相关题目
W、X、Y、Z是短周期元素,其部分性质如下表
W | X | Y | Z |
单质是淡黄色固体 | 与W同周期,其单质常用作半导体材料 | 原子最外层电子数是电子总数的2/3 | 第三周期原子半径最小的金属元素 |
下列说法正确的是( )
A.气态氢化物的热稳定性:X>W
B.最高价氧化物对应水化物的酸性:Y>X
C.简单离子半径:Z>W
D.工业上用Y单质还原Z的氧化物得Z的单质


 bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡时混合气体中G的体积分数。据此可判断( )
bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡时混合气体中G的体积分数。据此可判断( )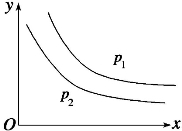
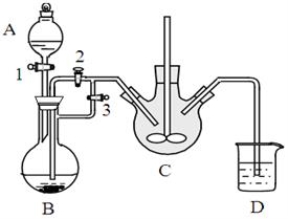
 刷电路板上的铜,所得的溶液中加入铁粉,对加入铁粉充分反应后的溶液分析合理的是( )
刷电路板上的铜,所得的溶液中加入铁粉,对加入铁粉充分反应后的溶液分析合理的是( )