题目内容
已知:合成氨是一个放热反应,下列事实不能用勒沙特列原理来解释的是( )
分析:勒沙特列原理是如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动,勒沙特列原理适用的对象应存在可逆过程,如与可逆过程无关,与平衡移动无关,则不能用勒沙特列原理解释.
解答:解:A.存在平衡2SO2+O2(g)?2SO3(g),正反应为气体体积减小的反应,增大压强,平衡向正反应移动,有利于合成SO3,能用勒沙特列原理解释,故A不选;
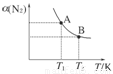
B.存在平衡2N2+3H2?2NH3,合成氨是放热过程,高温不利于氨气的合成,选择500℃考虑反应速率较快、且催化剂活性较高,故B选;
C.氨气液化,氨气的浓度降低,平衡向合成氨的方向移动,能用勒沙特列原理解释,故C不选;
D.过量空气煅烧硫铁矿,增大氧气的浓度,有利于反应向生成二氧化硫的方向移动,可以提高原料,能用勒沙特列原理解释,故D不选;
故选B.
B.存在平衡2N2+3H2?2NH3,合成氨是放热过程,高温不利于氨气的合成,选择500℃考虑反应速率较快、且催化剂活性较高,故B选;
C.氨气液化,氨气的浓度降低,平衡向合成氨的方向移动,能用勒沙特列原理解释,故C不选;
D.过量空气煅烧硫铁矿,增大氧气的浓度,有利于反应向生成二氧化硫的方向移动,可以提高原料,能用勒沙特列原理解释,故D不选;
故选B.
点评:本题考查勒夏特列原理知识,题目难度不大,注意使用勒夏特列原理的前提必须是可逆反应,且是否发生平衡的移动.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案 名题金卷系列答案
名题金卷系列答案
相关题目
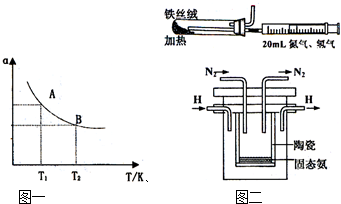 (2009?清远模拟)德国人哈伯在1909年发明的合成氨反应原理为:N2(g)+3H2(g)?2NH3(g) 已知298K时:△H=-92.4kJ?mol-1试回答下列问题:
(2009?清远模拟)德国人哈伯在1909年发明的合成氨反应原理为:N2(g)+3H2(g)?2NH3(g) 已知298K时:△H=-92.4kJ?mol-1试回答下列问题: 2NH3(g);已知298 K时,
2NH3(g);已知298 K时,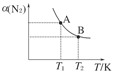
 2NH3(g);已知298 K时,
2NH3(g);已知298 K时,