题目内容
【题目】下列实验的操作正确的是( )
实验 | 操作 | |
① | 验证淀粉已完全水解 | 向水解产物中加入新制的Cu(OH) 2 悬浊液,加热 |
② | 比较氯和硅的非金属性强弱 | 将盐酸滴入Na2SiO3溶液中 |
③ | 验证Na2SO3 已被氧化 | 取样品溶于水,先加足量盐酸酸化,然后再加BaCl2 溶液 |
④ | 比较水和乙醇中羟基氢的活泼性 | 颗粒大小相同的钠分别与水和乙醇反应 |
⑤ | 除去乙酸乙酯中的乙酸、乙醇 | 加入足量饱和Na2CO3溶液,振荡、静置分液 |
⑥ | 验证用稀硝酸能将Fe 氧化成Fe3 + | 稀硝酸加入过量铁粉中,充分反应后滴加KSCN 溶液 |
A. ③ ④ ⑤ B. ① ② ⑥ C. ③ ⑤ ⑥ D. ① ③ ④
【答案】A
【解析】![]() 验证淀粉已完全水解必须选用碘水,若加入碘水不变蓝,则水解完全,选项①错误;②盐酸不是氯的最高价氧化物的水化物,无法比较氯和硅的非金属性强弱,选项②错误;③取样品溶于水,先加足量盐酸酸化,然后再加BaCl2 溶液,若产生白色沉淀,则说明Na2SO3 已被氧化,选项③正确;④颗粒大小相同的钠分别与水和乙醇反应,与水反应更剧烈,从而可以比较水和乙醇中羟基氢的活泼性,选项④正确;⑤加入足量饱和Na2CO3溶液,振荡、静置分液,可除去乙酸乙酯中的乙酸、乙醇,选项⑤正确;⑥稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液,溶液不显血红色,无法验证用稀硝酸能将Fe 氧化成Fe3 +,若稀硝酸过量则可以,选项⑥错误。答案选A。
验证淀粉已完全水解必须选用碘水,若加入碘水不变蓝,则水解完全,选项①错误;②盐酸不是氯的最高价氧化物的水化物,无法比较氯和硅的非金属性强弱,选项②错误;③取样品溶于水,先加足量盐酸酸化,然后再加BaCl2 溶液,若产生白色沉淀,则说明Na2SO3 已被氧化,选项③正确;④颗粒大小相同的钠分别与水和乙醇反应,与水反应更剧烈,从而可以比较水和乙醇中羟基氢的活泼性,选项④正确;⑤加入足量饱和Na2CO3溶液,振荡、静置分液,可除去乙酸乙酯中的乙酸、乙醇,选项⑤正确;⑥稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液,溶液不显血红色,无法验证用稀硝酸能将Fe 氧化成Fe3 +,若稀硝酸过量则可以,选项⑥错误。答案选A。

【题目】在密闭容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g) ![]() 2C(g);△H<0。达到平衡后,改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是
2C(g);△H<0。达到平衡后,改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是
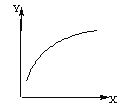
X | Y | |
A | 再加入A | B的百分含量 |
B | 再加入C | A的体积分数 |
C | 增大压强 | A的转化率 |
D | 升高高温度 | 混合气体平均摩尔质量 |
A. A B. B C. C D. D



